

A força de contração de qualquer comprimento de unidade na superfície do líquido é chamada de tensão superficial, e a unidade é N.·m-1.

A propriedade de reduzir a tensão superficial do solvente é chamada de atividade de superfície, e uma substância com essa propriedade é chamada de substância ativa de superfície.
A substância tensoativa que pode ligar moléculas em solução aquosa e formar micelas e outras associações, e ter alta atividade de superfície, além de ter o efeito de umectação, emulsificação, formação de espuma, lavagem, etc., é chamada de surfactante.
Surfactantes são compostos orgânicos com estrutura e propriedades especiais, que podem alterar significativamente a tensão interfacial entre duas fases ou a tensão superficial de líquidos (geralmente água), com umectação, formação de espuma, emulsificação, lavagem e outras propriedades.
Em termos de estrutura, os surfactantes têm uma característica comum, pois contêm dois grupos de natureza diferente em suas moléculas.Em uma extremidade está uma longa cadeia de grupo apolar, solúvel em óleo e insolúvel em água, também conhecido como grupo hidrofóbico ou grupo hidrorrepelente.Esse grupo repelente de água é geralmente cadeias longas de hidrocarbonetos, às vezes também para flúor orgânico, silício, organofosfato, cadeia de organoestanho, etc. Na outra extremidade está o grupo solúvel em água, um grupo hidrofílico ou grupo repelente de óleo.O grupo hidrofílico deve ser suficientemente hidrofílico para garantir que todos os surfactantes sejam solúveis em água e tenham a solubilidade necessária.Como os surfactantes contêm grupos hidrofílicos e hidrofóbicos, eles podem ser solúveis em pelo menos uma das fases líquidas.Essa propriedade hidrofílica e lipofílica do surfactante é chamada de anfifilicidade.


O surfactante é um tipo de moléculas anfifílicas com grupos hidrofóbicos e hidrofílicos.Grupos hidrofóbicos de surfactantes são geralmente compostos de hidrocarbonetos de cadeia longa, como alquil C8~C20 de cadeia linear, alquil C8~C20 de cadeia ramificada, alquilfenil (o número de tom de carbono do alquil é 8~16) e semelhantes.A diferença que é pequena entre os grupos hidrofóbicos está principalmente nas mudanças estruturais das cadeias de hidrocarbonetos.E os tipos de grupos hidrofílicos são mais, então as propriedades dos surfactantes estão relacionadas principalmente aos grupos hidrofílicos, além do tamanho e forma dos grupos hidrofóbicos.As mudanças estruturais dos grupos hidrofílicos são maiores do que as dos grupos hidrofóbicos, então a classificação dos surfactantes é geralmente baseada na estrutura dos grupos hidrofílicos.Essa classificação é baseada em se o grupo hidrofílico é iônico ou não, e é dividido em aniônicos, catiônicos, não iônicos, zwitteriônicos e outros tipos especiais de surfactantes.

① Adsorção de surfactantes na interface
As moléculas de surfactante são moléculas anfifílicas com grupos lipofílicos e hidrofílicos.Quando o surfactante é dissolvido em água, seu grupo hidrofílico é atraído pela água e se dissolve na água, enquanto seu grupo lipofílico é repelido pela água e sai da água, resultando na adsorção de moléculas (ou íons) do surfactante na interface das duas fases , o que reduz a tensão interfacial entre as duas fases.Quanto mais moléculas de surfactante (ou íons) forem adsorvidas na interface, maior será a redução na tensão interfacial.
② Algumas propriedades da membrana de adsorção
Pressão da superfície da membrana de adsorção: Adsorção do surfactante na interface gás-líquido para formar uma membrana de adsorção, como colocar uma folha flutuante removível sem fricção na interface, a folha flutuante empurra a membrana adsorvente ao longo da superfície da solução e a membrana gera uma pressão na folha flutuante, que é chamada de pressão de superfície.
Viscosidade superficial: Como a pressão superficial, a viscosidade superficial é uma propriedade exibida pela membrana molecular insolúvel.Suspenso por um anel de platina de fio de metal fino, de modo que seu plano entre em contato com a superfície da água do tanque, gire o anel de platina, o anel de platina pela viscosidade do impedimento da água, a amplitude diminui gradualmente, de acordo com a qual a viscosidade da superfície pode ser medido.O método é: primeiro, o experimento é conduzido na superfície da água pura para medir o decaimento da amplitude e, em seguida, o decaimento após a formação da membrana superficial é medido, e a viscosidade da membrana superficial é derivada da diferença entre os dois .
A viscosidade da superfície está intimamente relacionada à solidez da membrana da superfície e, como a membrana de adsorção tem pressão e viscosidade na superfície, ela deve ter elasticidade.Quanto maior a pressão superficial e maior a viscosidade da membrana adsorvida, maior o seu módulo de elasticidade.O módulo de elasticidade da membrana de adsorção de superfície é importante no processo de estabilização de bolhas.
③ Formação de micelas
Soluções diluídas de surfactantes obedecem às leis seguidas por soluções ideais.A quantidade de surfactante adsorvida na superfície da solução aumenta com a concentração da solução, e quando a concentração atinge ou excede um certo valor, a quantidade de adsorção não aumenta mais, e essas moléculas de surfactante em excesso ficam na solução de forma aleatória forma ou de alguma forma regular.Tanto a prática quanto a teoria mostram que eles formam associações em solução, e essas associações são chamadas de micelas.
Concentração Micelar Crítica (CMC): A concentração mínima na qual os surfactantes formam micelas em solução é chamada de concentração micelar crítica.
④ Valores de CMC de surfactantes comuns.

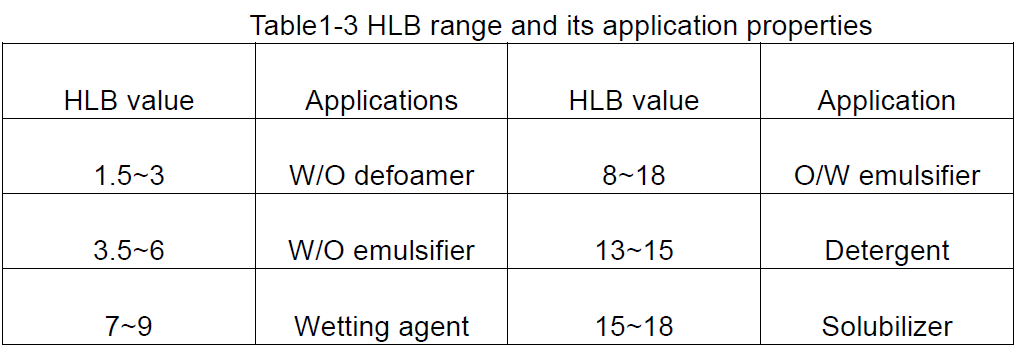
HLB é a abreviação de hydrophile lipophile balance, que indica o equilíbrio hidrofílico e lipofílico dos grupos hidrofílicos e lipofílicos do surfactante, ou seja, o valor de HLB do surfactante.Um grande valor de HLB indica uma molécula com forte hidrofilicidade e fraca lipofilicidade;inversamente, lipofilicidade forte e hidrofilicidade fraca.
① Provisões de valor HLB
O valor HLB é um valor relativo, portanto, quando o valor HLB é desenvolvido, como padrão, o valor HLB da parafina, que não possui propriedades hidrofílicas, é especificado como 0, enquanto o valor HLB do dodecil sulfato de sódio, que é mais solúvel em água, é 40. Portanto, o valor de HLB dos surfactantes geralmente está na faixa de 1 a 40. De modo geral, emulsificantes com valores de HLB menores que 10 são lipofílicos, enquanto aqueles maiores que 10 são hidrofílicos.Assim, o ponto de viragem de lipofílico para hidrofílico é de cerca de 10.
Com base nos valores de HLB dos surfactantes, pode-se obter uma ideia geral de seus possíveis usos, conforme mostrado na Tabela 1-3.

Dois líquidos mutuamente insolúveis, um disperso no outro como partículas (gotículas ou cristais líquidos) formam um sistema denominado emulsão.Este sistema é termodinamicamente instável devido ao aumento da área de contorno dos dois líquidos quando a emulsão é formada.Para tornar a emulsão estável, é necessário adicionar um terceiro componente - emulsificante para reduzir a energia interfacial do sistema.O emulsificante pertence ao surfactante, sua principal função é desempenhar o papel de emulsão.A fase da emulsão que existe como gotículas é chamada de fase dispersa (ou fase interna, fase descontínua), e a outra fase que está ligada entre si é chamada de meio de dispersão (ou fase externa, fase contínua).
① Emulsificantes e emulsões
Emulsões comuns, uma fase é água ou solução aquosa, a outra fase são substâncias orgânicas não miscíveis com água, como graxa, cera, etc. A emulsão formada por água e óleo pode ser dividida em dois tipos de acordo com sua situação de dispersão: óleo dispersa em água para formar emulsão do tipo óleo em água, expressa em O/A (óleo/água): água dispersa em óleo para formar emulsão do tipo óleo em água, expressa em A/O (água/óleo).Multiemulsões complexas água-em-óleo-em-água A/O/A e óleo-em-água-em-óleo O/A/O também podem ser formadas.
Emulsificantes são usados para estabilizar emulsões reduzindo a tensão interfacial e formando uma membrana interfacial de molécula única.
Na emulsificação dos requisitos do emulsificante:
a: O emulsificante deve ser capaz de adsorver ou enriquecer a interface entre as duas fases, de forma que a tensão interfacial seja reduzida;
b: O emulsificante deve ceder as partículas à carga, de modo que haja repulsão eletrostática entre as partículas, ou forme uma membrana protetora estável e altamente viscosa ao redor das partículas.
Portanto, a substância utilizada como emulsificante deve possuir grupos anfifílicos para emulsificar, e os tensoativos podem atender a esse requisito.
② Métodos de preparação de emulsões e fatores que afetam a estabilidade de emulsões
Existem duas maneiras de preparar emulsões: uma é usar o método mecânico para dispersar o líquido em minúsculas partículas em outro líquido, que é mais usado na indústria para preparar emulsões;a outra é dissolver o líquido em estado molecular em outro líquido, e depois fazer com que ele se reúna adequadamente para formar emulsões.
A estabilidade de uma emulsão é a capacidade de agregação de antipartículas que leva à separação de fases.Emulsões são sistemas termodinamicamente instáveis com grande energia livre.Portanto, a chamada estabilidade de uma emulsão é, na verdade, o tempo necessário para que o sistema atinja o equilíbrio, ou seja, o tempo necessário para que ocorra a separação de um dos líquidos do sistema.
Quando a membrana interfacial com álcoois graxos, ácidos graxos e aminas graxas e outras moléculas orgânicas polares, a resistência da membrana é significativamente maior.Isso ocorre porque, na camada de adsorção interfacial de moléculas emulsificantes e álcoois, ácidos e aminas e outras moléculas polares para formar um "complexo", de modo que a resistência da membrana interfacial aumentou.
Os emulsificantes que consistem em mais de dois surfactantes são chamados de emulsificantes mistos.Emulsificante misto adsorvido na interface água/óleo;ação intermolecular pode formar complexos.Devido à forte ação intermolecular, a tensão interfacial é significativamente reduzida, a quantidade de emulsificante adsorvido na interface é significativamente aumentada, a formação de densidade de membrana interfacial aumenta, a força aumenta.
A carga das esferas líquidas tem um efeito significativo na estabilidade da emulsão.Emulsões estáveis, cujos grânulos líquidos são geralmente carregados.Quando se utiliza um emulsificante iônico, o íon emulsificante adsorvido na interface tem seu grupo lipofílico inserido na fase oleosa e o grupo hidrofílico está na fase aquosa, tornando os grânulos líquidos carregados.Como os grânulos de emulsão com a mesma carga, eles se repelem, não são fáceis de aglomerar, de modo que a estabilidade é aumentada.Pode-se observar que quanto mais íons emulsificantes adsorvidos nos grânulos, maior a carga, maior a capacidade de impedir a aglomeração dos grânulos, mais estável o sistema de emulsão.
A viscosidade do meio de dispersão da emulsão tem uma certa influência na estabilidade da emulsão.Geralmente, quanto maior a viscosidade do meio de dispersão, maior a estabilidade da emulsão.Isso ocorre porque a viscosidade do meio de dispersão é grande, o que tem um forte efeito no movimento browniano das esferas líquidas e retarda a colisão entre as esferas líquidas, de modo que o sistema permaneça estável.Normalmente, as substâncias poliméricas que podem ser dissolvidas em emulsões podem aumentar a viscosidade do sistema e aumentar a estabilidade das emulsões.Além disso, os polímeros também podem formar uma forte membrana interfacial, tornando o sistema de emulsão mais estável.
Em alguns casos, a adição de pó sólido também pode fazer com que a emulsão tenda a se estabilizar.O pó sólido está na água, óleo ou interface, dependendo do óleo, água na capacidade de umedecimento do pó sólido, se o pó sólido não estiver completamente molhado com água, mas também molhado com óleo, permanecerá na água e no óleo interface.
O pó sólido não torna a emulsão estável porque o pó reunido na interface aumenta a membrana interfacial, que é semelhante à adsorção interfacial das moléculas do emulsificante; portanto, quanto mais próximo o material sólido do pó estiver disposto na interface, mais estável será emulsão é.
Os surfactantes têm a capacidade de aumentar significativamente a solubilidade de substâncias orgânicas insolúveis ou pouco solúveis em água após a formação de micelas em solução aquosa, e a solução é transparente neste momento.Este efeito da micela é chamado de solubilização.O surfactante que pode produzir solubilização é chamado de solubilizante, e a matéria orgânica que é solubilizada é chamada de matéria solubilizada.

A espuma desempenha um papel importante no processo de lavagem.Espuma é um sistema de dispersão no qual um gás é disperso em um líquido ou sólido, tendo o gás como fase dispersa e o líquido ou sólido como meio dispersante, sendo a primeira chamada de espuma líquida, enquanto a segunda é chamada de espuma sólida, tal como espuma de plástico, espuma de vidro, espuma de cimento, etc.
(1) Formação de espuma
Por espuma entendemos aqui um agregado de bolhas de ar separadas por uma membrana líquida.Esse tipo de bolha sempre sobe rapidamente para a superfície do líquido devido à grande diferença de densidade entre a fase dispersa (gás) e o meio de dispersão (líquido), aliada à baixa viscosidade do líquido.
O processo de formação de uma bolha consiste em trazer uma grande quantidade de gás para o líquido, e as bolhas no líquido retornam rapidamente à superfície, formando um agregado de bolhas separadas por uma pequena quantidade de gás líquido.
A espuma tem duas características importantes em termos de morfologia: uma é que as bolhas como uma fase dispersa são frequentemente de forma poliédrica, isso porque na interseção das bolhas, há uma tendência para o filme líquido se tornar mais fino, de modo que as bolhas se tornem poliédrica, quando o filme líquido afina até certo ponto, leva à ruptura das bolhas;a segunda é que líquidos puros não podem formar espuma estável, o líquido que pode formar espuma tem pelo menos dois ou mais componentes.As soluções aquosas de tensoativos são típicas de sistemas propensos à formação de espuma, e sua capacidade de gerar espuma também está relacionada a outras propriedades.
Os surfactantes com bom poder espumante são chamados de agentes espumantes.Embora o agente espumante tenha boa capacidade de formação de espuma, a espuma formada pode não ser capaz de se manter por muito tempo, ou seja, sua estabilidade não é necessariamente boa.A fim de manter a estabilidade da espuma, muitas vezes no agente espumante para adicionar substâncias que podem aumentar a estabilidade da espuma, a substância é chamada de estabilizador de espuma, o estabilizador comumente usado é lauril dietanolamina e óxido de dodecil dimetilamina.
(2) Estabilidade da espuma
A espuma é um sistema termodinamicamente instável e a tendência final é que a área de superfície total do líquido dentro do sistema diminui depois que a bolha é quebrada e a energia livre diminui.O processo de desespumação é o processo pelo qual a membrana líquida que separa o gás torna-se cada vez mais espessa até se romper.Portanto, o grau de estabilidade da espuma é determinado principalmente pela velocidade de descarga do líquido e pela resistência do filme líquido.Os seguintes fatores também influenciam isso.
(3) Destruição de espuma
O princípio básico da destruição da espuma é alterar as condições que produzem a espuma ou eliminar os fatores estabilizadores da espuma, portanto, existem métodos físicos e químicos de desespumação.
A desespumação física significa alterar as condições de produção de espuma, mantendo a composição química da solução de espuma, como distúrbios externos, mudanças de temperatura ou pressão e tratamento ultrassônico são métodos físicos eficazes para eliminar a espuma.
O método de desespumação química é adicionar certas substâncias para interagir com o agente espumante para reduzir a resistência do filme líquido na espuma e, assim, reduzir a estabilidade da espuma para atingir o objetivo de desespuma, tais substâncias são chamadas de antiespumantes.A maioria dos antiespumantes são surfactantes.Portanto, de acordo com o mecanismo de desespumação, o antiespumante deve ter uma forte capacidade de reduzir a tensão superficial, fácil de adsorver na superfície, e a interação entre as moléculas de adsorção da superfície é fraca, as moléculas de adsorção dispostas em uma estrutura mais solta.
Existem vários tipos de antiespumantes, mas basicamente são todos surfactantes não iônicos.Os surfactantes não iônicos têm propriedades antiespumantes próximas ou acima de seu ponto de névoa e são freqüentemente usados como antiespumantes.Álcoois, especialmente álcoois com estrutura ramificada, ácidos graxos e ésteres de ácidos graxos, poliamidas, ésteres de fosfato, óleos de silicone, etc. também são comumente usados como excelentes antiespumantes.
(4) Espuma e lavagem
Não há ligação direta entre a espuma e a eficácia da lavagem e a quantidade de espuma não indica a eficácia da lavagem.Por exemplo, os surfactantes não iônicos têm muito menos propriedades espumantes do que os sabões, mas sua descontaminação é muito melhor do que os sabões.
Em alguns casos, a espuma pode ser útil na remoção de sujeira e sujeira.Por exemplo, ao lavar a loiça em casa, a espuma do detergente recolhe as gotas de óleo e ao esfregar tapetes, a espuma ajuda a recolher o pó, o pó e outras sujidades sólidas.Além disso, a espuma às vezes pode ser usada como uma indicação da eficácia de um detergente.Como os óleos gordurosos têm um efeito inibidor na espuma do detergente, quando há muito óleo e pouco detergente, nenhuma espuma será gerada ou a espuma original desaparecerá.Às vezes, a espuma também pode ser usada como um indicador da limpeza de um enxágue, pois a quantidade de espuma na solução de enxágue tende a diminuir com a redução do detergente, portanto, a quantidade de espuma pode ser usada para avaliar o grau de enxágue.
Em um sentido amplo, a lavagem é o processo de remover componentes indesejados do objeto a ser lavado e atingir algum objetivo.A lavagem no sentido usual refere-se ao processo de remoção da sujeira da superfície do transportador.Na lavagem, a interação entre a sujeira e o portador é enfraquecida ou eliminada pela ação de algumas substâncias químicas (por exemplo, detergente, etc.), de modo que a combinação de sujeira e portador é alterada para a combinação de sujeira e detergente, e finalmente a sujeira é separada do transportador.Como os objetos a serem lavados e a sujeira a ser removida são diversos, a lavagem é um processo muito complexo e o processo básico de lavagem pode ser expresso nas seguintes relações simples.
Transportador··Sujeira + Detergente= Transportador + Sujeira·Detergente
O processo de lavagem costuma ser dividido em duas etapas: na primeira, sob a ação do detergente, a sujeira é separada de seu portador;em segundo lugar, a sujeira destacada é dispersa e suspensa no meio.O processo de lavagem é um processo reversível e a sujeira dispersa e suspensa no meio também pode ser precipitada novamente do meio para o objeto a ser lavado.Portanto, um bom detergente deve ter a capacidade de dispersar e suspender a sujeira e evitar a redeposição de sujeira, além da capacidade de remover a sujeira do transportador.
(1) Tipos de sujeira
Mesmo para um mesmo item, o tipo, a composição e a quantidade de sujeira podem variar de acordo com o ambiente em que é utilizado.A sujeira do corpo de óleo é principalmente alguns óleos animais e vegetais e óleos minerais (como petróleo bruto, óleo combustível, alcatrão de carvão, etc.), a sujeira sólida é principalmente fuligem, cinzas, ferrugem, negro de fumo, etc. há sujeira do corpo humano, como suor, sebo, sangue, etc .;sujeira de alimentos, como manchas de frutas, manchas de óleo de cozinha, manchas de condimentos, goma, etc.;sujeira de cosméticos, como batom, esmalte de unha, etc.;sujeira da atmosfera, como fuligem, poeira, lama, etc.;outros, como tinta, chá, revestimento, etc. Existem vários tipos.
Os vários tipos de sujeira geralmente podem ser divididos em três categorias principais: sujeira sólida, sujeira líquida e sujeira especial.
① Sujeira sólida
A sujeira sólida comum inclui partículas de cinzas, lama, terra, ferrugem e negro de fumo.A maioria dessas partículas tem uma carga elétrica em sua superfície, a maioria delas são carregadas negativamente e podem ser facilmente adsorvidas em itens de fibra.Sujeira sólida geralmente é difícil de dissolver na água, mas pode ser dispersa e suspensa por soluções detergentes.Sujeira sólida com ponto de massa menor é mais difícil de remover.
② Sujeira líquida
A sujeira líquida é principalmente solúvel em óleo, incluindo óleos vegetais e animais, ácidos graxos, álcoois graxos, óleos minerais e seus óxidos.Entre eles, óleos vegetais e animais, ácidos graxos e saponificação alcalina podem ocorrer, enquanto álcoois graxos, óleos minerais não são saponificados por álcalis, mas podem ser solúveis em álcoois, éteres e solventes orgânicos de hidrocarbonetos, emulsificação e dispersão de solução de água detergente.A sujeira líquida solúvel em óleo geralmente tem uma forte força com itens de fibra e é mais firmemente adsorvida nas fibras.
③ Sujeira especial
A sujeira especial inclui proteínas, amido, sangue, secreções humanas como suor, sebo, urina e suco de frutas e suco de chá.A maior parte desse tipo de sujeira pode ser quimicamente e fortemente adsorvida em itens de fibra.Portanto, é difícil de lavar.
Os vários tipos de sujeira raramente são encontrados sozinhos, mas muitas vezes são misturados e adsorvidos no objeto.Às vezes, a sujeira pode ser oxidada, decomposta ou deteriorada sob influências externas, criando assim nova sujeira.
(2) Aderência de sujeira
Roupas, mãos etc. podem ficar manchadas porque existe algum tipo de interação entre o objeto e a sujeira.A sujeira adere aos objetos de várias maneiras, mas não há mais do que adesões físicas e químicas.
①A adesão de fuligem, poeira, lama, areia e carvão à roupa é uma adesão física.De um modo geral, através desta adesão de sujeira, e o papel entre o objeto manchado é relativamente fraco, a remoção de sujeira também é relativamente fácil.De acordo com as diferentes forças, a adesão física da sujeira pode ser dividida em adesão mecânica e adesão eletrostática.
A: Adesão mecânica
Este tipo de adesão refere-se principalmente à adesão de alguma sujidade sólida (por exemplo, pó, lama e areia).A adesão mecânica é uma das formas mais fracas de adesão de sujeira e pode ser removida quase por meios puramente mecânicos, mas quando a sujeira é pequena (<0,1um), é mais difícil de remover.
B:Adesão eletrostática
A adesão eletrostática se manifesta principalmente na ação de partículas de sujeira carregadas em objetos com cargas opostas.A maioria dos objetos fibrosos são carregados negativamente na água e podem ser facilmente aderidos por certas sujeiras carregadas positivamente, como tipos de cal.Algumas sujeiras, embora carregadas negativamente, como partículas de negro de fumo em soluções aquosas, podem aderir às fibras através de pontes iônicas (íons entre múltiplos objetos de cargas opostas, agindo em conjunto com eles como uma ponte) formadas por íons positivos na água (ex. , Ca2+, Mg2+ etc.).
A ação eletrostática é mais forte do que a ação mecânica simples, tornando a remoção de sujeira relativamente difícil.
② Adesão química
A adesão química refere-se ao fenômeno da sujeira agindo sobre um objeto por meio de ligações químicas ou de hidrogênio.Por exemplo, sujeira sólida polar, proteína, ferrugem e outras aderências em itens de fibra, fibras contêm carboxila, hidroxila, amida e outros grupos, esses grupos e ácidos graxos de sujeira oleosa, álcoois graxos são fáceis de formar ligações de hidrogênio.As forças químicas são geralmente fortes e, portanto, a sujeira é mais firmemente ligada ao objeto.Este tipo de sujeira é difícil de remover pelos métodos usuais e requer métodos especiais para lidar com ela.
O grau de aderência da sujeira está relacionado à natureza da própria sujeira e à natureza do objeto ao qual está aderida.Geralmente, as partículas aderem facilmente a itens fibrosos.Quanto menor a textura da sujeira sólida, mais forte a adesão.A sujeira polar em objetos hidrofílicos, como algodão e vidro, adere mais fortemente do que a sujeira apolar.A sujeira não polar adere mais fortemente do que a sujeira polar, como gorduras polares, poeira e argila, e é menos fácil de remover e limpar.
(3) Mecanismo de remoção de sujeira
O objetivo da lavagem é remover a sujeira.Em um meio de uma certa temperatura (principalmente água).Usando os vários efeitos físicos e químicos do detergente para enfraquecer ou eliminar o efeito da sujeira e objetos lavados, sob a ação de certas forças mecânicas (como esfregar as mãos, agitação da máquina de lavar, impacto da água), para que a sujeira e os objetos lavados do propósito de descontaminação.
① Mecanismo de remoção de sujeira líquida
A: Umectante
A sujeira líquida é principalmente à base de óleo.As manchas de óleo molham a maioria dos itens fibrosos e se espalham mais ou menos como uma película de óleo na superfície do material fibroso.O primeiro passo na ação de lavagem é o umedecimento da superfície pelo líquido de lavagem.Para fins de ilustração, a superfície de uma fibra pode ser considerada como uma superfície lisa e sólida.
B: Descolamento de óleo - mecanismo de ondulação
A segunda etapa da ação de lavagem é a remoção do óleo e da graxa, a remoção da sujeira líquida é realizada por meio de uma espécie de enrolamento.A sujeira líquida existia originalmente na superfície na forma de uma película de óleo espalhada e, sob o efeito umectante preferencial do líquido de lavagem na superfície sólida (ou seja, a superfície da fibra), ela se enrolou em gotas de óleo passo a passo, que foram substituídos pelo líquido de lavagem e eventualmente deixaram a superfície sob certas forças externas.
② Mecanismo de remoção de sujeira sólida
A remoção da sujeira líquida se dá principalmente através do umedecimento preferencial da sujeira carreadora pela solução de lavagem, enquanto o mecanismo de remoção da sujeira sólida é diferente, onde o processo de lavagem consiste principalmente no umedecimento da massa de sujeira e sua superfície carreadora pela lavagem solução.Devido à adsorção de tensoativos na sujeira sólida e sua superfície transportadora, a interação entre a sujeira e a superfície é reduzida e a força de adesão da massa de sujeira na superfície é reduzida, assim a massa de sujeira é facilmente removida da superfície de o transportador.
Além disso, a adsorção de surfactantes, especialmente surfactantes iônicos, na superfície da sujeira sólida e seu transportador tem o potencial de aumentar o potencial de superfície na superfície da sujeira sólida e seu transportador, o que é mais propício para a remoção do sujeira.Superfícies sólidas ou geralmente fibrosas são geralmente carregadas negativamente em meios aquosos e podem, portanto, formar camadas eletrônicas duplas difusas em massas de sujeira ou superfícies sólidas.Devido à repulsão de cargas homogêneas, a adesão de partículas de sujeira na água à superfície sólida é enfraquecida.Quando um surfactante aniônico é adicionado, porque pode aumentar simultaneamente o potencial negativo da superfície da partícula de sujeira e da superfície sólida, a repulsão entre eles é mais aprimorada, a força de adesão da partícula é mais reduzida e a sujeira é mais fácil de remover .
Os surfactantes não iônicos são adsorvidos em superfícies sólidas geralmente carregadas e, embora não alterem significativamente o potencial interfacial, os surfactantes não iônicos adsorvidos tendem a formar uma certa espessura de camada adsorvida na superfície, o que ajuda a evitar a redeposição de sujeira.
No caso dos tensoativos catiônicos, sua adsorção reduz ou elimina o potencial negativo de superfície da massa de sujeira e sua superfície portadora, o que reduz a repulsão entre a sujeira e a superfície e, portanto, não favorece a remoção de sujeira;além disso, após a adsorção na superfície sólida, os surfactantes catiônicos tendem a tornar a superfície sólida hidrofóbica e, portanto, não conduzem à umectação da superfície e, portanto, à lavagem.
③ Remoção de solos especiais
Proteína, amido, secreções humanas, suco de frutas, suco de chá e outras sujeiras semelhantes são difíceis de remover com surfactantes normais e requerem tratamento especial.
Manchas de proteínas como creme, ovos, sangue, leite e excrementos de pele tendem a coagular nas fibras e degenerar e obter adesão mais forte.Sujeira de proteína pode ser removida usando proteases.A enzima protease decompõe as proteínas da sujeira em aminoácidos solúveis em água ou oligopeptídeos.
As manchas de amido provêm principalmente de alimentos, outros como molho, cola, etc. A amilase tem um efeito catalítico na hidrólise das manchas de amido, fazendo com que o amido se decomponha em açúcares.
A lipase catalisa a decomposição dos triglicerídeos, que são difíceis de remover por métodos normais, como sebo e óleos comestíveis, e os decompõe em glicerol solúvel e ácidos graxos.
Algumas manchas coloridas de sucos de frutas, sucos de chá, tintas, batons etc. geralmente são difíceis de limpar completamente, mesmo após lavagens repetidas.Essas manchas podem ser removidas por uma reação redox com um agente oxidante ou redutor, como alvejante, que destrói a estrutura dos grupos geradores de cor ou auxiliares de cor e os degrada em componentes solúveis em água menores.
(4) Mecanismo de remoção de manchas de limpeza a seco
O acima é realmente para água como meio de lavagem.De fato, devido aos diferentes tipos de roupas e estrutura, algumas roupas que usam lavagem com água não são convenientes ou fáceis de lavar, algumas roupas após a lavagem e até deformação, desbotamento, etc., por exemplo: a maioria das fibras naturais absorve água e fácil de inchar e secar e fácil de encolher, então após a lavagem será deformado;lavando produtos de lã também freqüentemente aparecem fenômeno de encolhimento, alguns produtos de lã com lavagem com água também são fáceis de borbulhar, mudança de cor;A sensação das mãos de algumas sedas piora após a lavagem e perde o brilho.Para essas roupas, muitas vezes, use o método de lavagem a seco para descontaminar.A chamada limpeza a seco geralmente se refere ao método de lavagem em solventes orgânicos, especialmente em solventes apolares.
A lavagem a seco é uma forma mais suave de lavagem do que a lavagem com água.Como a lavagem a seco não requer muita ação mecânica, não causa danos, rugas e deformações nas roupas, enquanto os agentes de limpeza a seco, ao contrário da água, raramente produzem expansão e contração.Desde que a tecnologia seja manejada adequadamente, as roupas podem ser lavadas a seco sem distorção, desbotamento da cor e vida útil prolongada.
Em termos de limpeza a seco, existem três grandes tipos de sujeira.
①Sujeira solúvel em óleo A sujeira solúvel em óleo inclui todos os tipos de óleo e graxa, que são líquidos ou gordurosos e podem ser dissolvidos em solventes de limpeza a seco.
②Sujeira solúvel em água A sujeira solúvel em água é solúvel em soluções aquosas, mas não em agentes de limpeza a seco, é adsorvida na roupa em estado aquoso, a água evapora após a precipitação de sólidos granulares, como sais inorgânicos, amido, proteínas, etc.
③Sujeira insolúvel em óleo e água A sujeira insolúvel em água e óleo não é solúvel em água nem em solventes de limpeza a seco, como negro de fumo, silicatos de vários metais e óxidos, etc.
Devido à natureza diferente dos vários tipos de sujidade, existem diferentes formas de remover a sujidade no processo de limpeza a seco.Sujeiras solúveis em óleo, como óleos animais e vegetais, óleos minerais e graxas, são facilmente solúveis em solventes orgânicos e podem ser removidas mais facilmente na lavagem a seco.A excelente solubilidade dos solventes de limpeza a seco para óleos e graxas vem essencialmente das forças de van der Walls entre as moléculas.
Para a remoção de sujeira solúvel em água, como sais inorgânicos, açúcares, proteínas e suor, também deve ser adicionada a quantidade certa de água ao agente de limpeza a seco, caso contrário, a sujeira solúvel em água é difícil de remover da roupa.No entanto, é difícil dissolver a água no agente de limpeza a seco, portanto, para aumentar a quantidade de água, você também precisa adicionar surfactantes.A presença de água no agente de limpeza a seco pode tornar a superfície da sujeira e da roupa hidratada, facilitando a interação com os grupos polares dos surfactantes, o que favorece a adsorção dos surfactantes na superfície.Além disso, quando os surfactantes formam micelas, sujeira solúvel em água e água podem ser solubilizadas nas micelas.Além de aumentar o teor de água do solvente de limpeza a seco, os surfactantes também podem desempenhar um papel na prevenção da redeposição de sujeira para aumentar o efeito de descontaminação.
A presença de uma pequena quantidade de água é necessária para remover a sujeira solúvel em água, mas muita água pode causar deformação e enrugamento em algumas roupas, por isso a quantidade de água no agente de limpeza a seco deve ser moderada.
Sujeira que não é solúvel em água nem solúvel em óleo, partículas sólidas como cinzas, lama, terra e negro de fumo, geralmente é presa à roupa por forças eletrostáticas ou em combinação com óleo.Na limpeza a seco, o fluxo de solvente, o impacto pode fazer com que a força eletrostática absorva a sujeira, e o agente de limpeza a seco pode dissolver o óleo, de modo que a combinação de óleo e sujeira e presa à roupa de partículas sólidas no seco - agente de limpeza, agente de limpeza a seco em uma pequena quantidade de água e surfactantes, para que as partículas sólidas de sujeira possam ser suspensão estável, dispersão, para evitar sua redeposição na roupa.
(5) Fatores que afetam a ação de lavagem
A adsorção direcional de surfactantes na interface e a redução da tensão superficial (interfacial) são os principais fatores na remoção de sujeira líquida ou sólida.No entanto, o processo de lavagem é complexo e o efeito de lavagem, mesmo com o mesmo tipo de detergente, é influenciado por muitos outros fatores.Esses fatores incluem a concentração do detergente, a temperatura, a natureza da sujeira, o tipo de fibra e a estrutura do tecido.
① Concentração de surfactante
As micelas de surfactantes em solução desempenham um papel importante no processo de lavagem.Quando a concentração atinge a concentração micelar crítica (CMC), o efeito de lavagem aumenta acentuadamente.Portanto, a concentração de detergente no solvente deve ser maior que o valor CMC para ter um bom efeito de lavagem.No entanto, quando a concentração de surfactante é maior do que o valor CMC, o aumento incremental no efeito de lavagem não é óbvio e não é necessário aumentar muito a concentração de surfactante.
Ao remover o óleo por solubilização, o efeito de solubilização aumenta com o aumento da concentração do surfactante, mesmo quando a concentração está acima do CMC.Neste momento, é aconselhável usar detergente de forma centralizada local.Por exemplo, se houver muita sujeira nos punhos e na gola de uma roupa, pode-se aplicar uma camada de detergente durante a lavagem para aumentar o efeito solubilizante do surfactante no óleo.
②A temperatura tem uma influência muito importante na ação de descontaminação.Em geral, o aumento da temperatura facilita a remoção da sujeira, mas às vezes uma temperatura muito alta também pode causar desvantagens.
O aumento da temperatura facilita a difusão da sujeira, a graxa sólida emulsifica-se facilmente em temperaturas acima de seu ponto de fusão e as fibras aumentam de inchamento devido ao aumento da temperatura, o que facilita a remoção da sujeira.No entanto, para tecidos compactos, os microgaps entre as fibras são reduzidos à medida que as fibras se expandem, o que é prejudicial para a remoção de sujeira.
As mudanças de temperatura também afetam a solubilidade, o valor CMC e o tamanho da micela dos surfactantes, afetando assim o efeito de lavagem.A solubilidade dos surfactantes com longas cadeias de carbono é baixa em baixas temperaturas e, às vezes, a solubilidade é ainda menor do que o valor CMC, portanto, a temperatura de lavagem deve ser aumentada adequadamente.O efeito da temperatura no valor de CMC e no tamanho da micela é diferente para surfactantes iônicos e não iônicos.Para surfactantes iônicos, um aumento na temperatura geralmente aumenta o valor de CMC e reduz o tamanho da micela, o que significa que a concentração de surfactante na solução de lavagem deve ser aumentada.Para surfactantes não iônicos, um aumento na temperatura leva a uma diminuição no valor CMC e um aumento significativo no volume da micela, então é claro que um aumento apropriado na temperatura ajudará o surfactante não iônico a exercer seu efeito tensoativo .No entanto, a temperatura não deve exceder seu ponto de névoa.
Resumindo, a temperatura ideal de lavagem depende da formulação do detergente e do objeto a ser lavado.Alguns detergentes têm um bom efeito detergente à temperatura ambiente, enquanto outros têm uma detergência muito diferente entre a lavagem a frio e a quente.
③ Espuma
Costuma-se confundir poder de espuma com efeito de lavagem, acreditando que detergentes com alto poder de espuma têm um bom efeito de lavagem.A pesquisa mostrou que não há relação direta entre o efeito de lavagem e a quantidade de espuma.Por exemplo, lavar com detergentes de baixa espuma não é menos eficaz do que lavar com detergentes de alta espuma.
Embora a espuma não esteja diretamente relacionada à lavagem, há ocasiões em que ajuda a remover a sujeira, por exemplo, ao lavar a louça à mão.Ao esfregar carpetes, a espuma também pode remover a poeira e outras partículas sólidas de sujeira, a sujeira do carpete é responsável por uma grande proporção de poeira, portanto, os agentes de limpeza do carpete devem ter uma certa capacidade de formação de espuma.
O poder espumante também é importante para xampus, onde a espuma fina produzida pelo líquido durante a lavagem ou banho deixa o cabelo lubrificado e confortável.
④ Variedades de fibras e propriedades físicas dos têxteis
Além da estrutura química das fibras, que afeta a adesão e remoção da sujeira, a aparência das fibras e a organização do fio e do tecido influenciam na facilidade de remoção da sujeira.
As escamas das fibras de lã e as fitas curvas e planas das fibras de algodão são mais propensas a acumular sujeira do que as fibras lisas.Por exemplo, o negro de fumo manchado em filmes de celulose (filmes de viscose) é fácil de remover, enquanto o negro de fumo manchado em tecidos de algodão é difícil de lavar.Outro exemplo é que os tecidos de fibra curta feitos de poliéster são mais propensos a acumular manchas de óleo do que os tecidos de fibra longa, e as manchas de óleo em tecidos de fibra curta também são mais difíceis de remover do que as manchas de óleo em tecidos de fibra longa.
Fios bem torcidos e tecidos apertados, devido ao pequeno espaço entre as fibras, podem resistir à invasão de sujeira, mas o mesmo também pode impedir que o líquido de lavagem exclua a sujeira interna, então tecidos apertados passam a resistir bem à sujeira, mas uma vez manchados lavar também é mais difícil.
⑤ Dureza da água
A concentração de Ca2+, Mg2+ e outros íons metálicos na água tem grande influência no efeito de lavagem, principalmente quando os tensoativos aniônicos encontram íons Ca2+ e Mg2+ formando sais de cálcio e magnésio que são menos solúveis e irão reduzir sua detergência.Em águas duras, mesmo que a concentração de surfactante seja alta, a detergência ainda é muito pior do que na destilação.Para que o surfactante tenha o melhor efeito de lavagem, a concentração de íons Ca2+ na água deve ser reduzida para 1 x 10-6 mol/L (CaCO3 para 0,1 mg/L) ou menos.Isso requer a adição de vários amaciantes ao detergente.
Horário de postagem: 25 de fevereiro de 2022



