Índice para este artigo:
1. Desenvolvimento de aminoácidos
2. Propriedades estruturais
3. Composição química
4.Classificação
5. Síntese
6. Propriedades físico -químicas
7. Toxicidade
8. Atividade antimicrobiana
9. Propriedades reológicas
10. Aplicações na indústria cosmética
11. Aplicações em cosméticos cotidianos
Surfactantes de aminoácidos (AAS)são uma classe de surfactantes formados pela combinação de grupos hidrofóbicos com um ou mais aminoácidos. Nesse caso, os aminoácidos podem ser sintéticos ou derivados de hidrolisados de proteínas ou fontes renováveis similares. Este artigo abrange os detalhes da maioria das rotas sintéticas disponíveis para o AAS e o efeito de diferentes rotas nas propriedades físico -químicas dos produtos finais, incluindo solubilidade, estabilidade de dispersão, toxicidade e biodegradabilidade. Como classe de surfactantes no aumento da demanda, a versatilidade do AAS devido à sua estrutura variável oferece um grande número de oportunidades comerciais.
Dado que os surfactantes são amplamente utilizados em detergentes, emulsificantes, inibidores de corrosão, recuperação de petróleo terciário e produtos farmacêuticos, os pesquisadores nunca deixaram de prestar atenção aos surfactantes.
Os surfactantes são os produtos químicos mais representativos que são consumidos em grandes quantidades diariamente em todo o mundo e tiveram um impacto negativo no ambiente aquático.Estudos mostraram que o uso generalizado de surfactantes tradicionais pode ter um impacto negativo no meio ambiente.
Hoje, a não toxicidade, biodegradabilidade e biocompatibilidade são quase tão importantes para os consumidores quanto a utilidade e o desempenho dos surfactantes.
Os biossurfactantes são surfactantes sustentáveis ambientalmente amigáveis que são naturalmente sintetizados por microorganismos como bactérias, fungos e leveduras ou secretados extracelularmente.Portanto, os biossurfactantes também podem ser preparados pelo projeto molecular para imitar estruturas anfifílicas naturais, como fosfolipídios, alquil glicosídeos e acil aminoácidos.
Surfactantes de aminoácidos (AAS)são um dos surfactantes típicos, geralmente produzidos a partir de matérias -primas derivadas de animais ou agrícolas. Nas últimas duas décadas, os AAs atraíram muito interesse dos cientistas como surfactantes novos, não apenas porque podem ser sintetizados a partir de recursos renováveis, mas também porque os AAs são prontamente degradáveis e têm subprodutos inofensivos, tornando-os mais seguros para o meio ambiente.
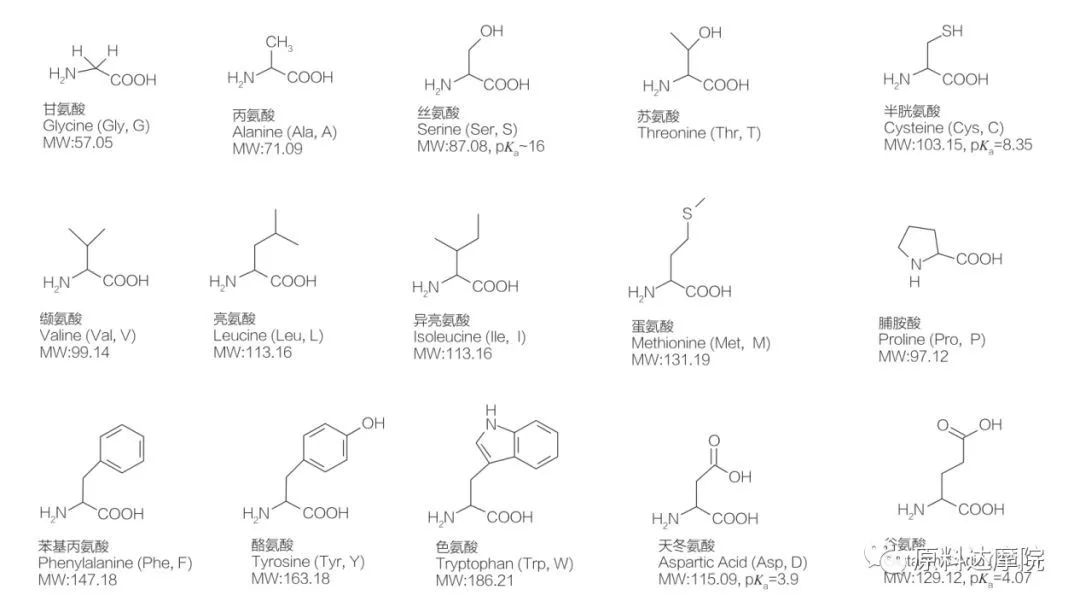
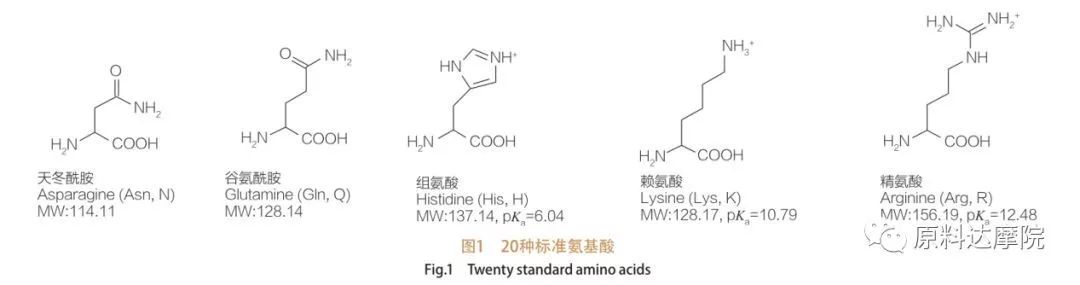
Os AAs podem ser definidos como uma classe de surfactantes que consistem em aminoácidos contendo grupos de aminoácidos (HO 2 C-ChR-NH 2) ou resíduos de aminoácidos (HO 2 C-Chr-NH-). As duas regiões funcionais de aminoácidos permitem a derivação de uma ampla variedade de surfactantes. Sabe -se que um total de 20 aminoácidos proteinogênicos padrão existe na natureza e é responsável por todas as reações fisiológicas nas atividades de crescimento e vida. Eles diferem um do outro apenas de acordo com o resíduo R (Figura 1, PK A é o logaritmo negativo da constante de dissociação ácida da solução). Alguns são não polares e hidrofóbicos, outros são polares e hidrofílicos, outros são básicos e outros são ácidos.
Como os aminoácidos são compostos renováveis, os surfactantes sintetizados a partir de aminoácidos também têm um alto potencial para se tornarem sustentáveis e ecológicos. A estrutura simples e natural, a baixa toxicidade e a rápida biodegradabilidade geralmente os tornam superiores aos surfactantes convencionais. Utilizando matérias -primas renováveis (por exemplo, aminoácidos e óleos vegetais), o AAS pode ser produzido por diferentes rotas biotecnológicas e rotas químicas.
No início do século XX, descobriu -se que os aminoácidos foram usados como substratos para a síntese de surfactantes.Os AAs foram usados principalmente como conservantes em formulações farmacêuticas e cosméticas.Além disso, verificou-se que os AAs são biologicamente ativos contra uma variedade de bactérias, tumores e vírus causadores de doenças. Em 1988, a disponibilidade de AAS de baixo custo gerou interesse de pesquisa na atividade da superfície. Hoje, com o desenvolvimento da biotecnologia, alguns aminoácidos também podem ser sintetizados comercialmente em larga escala por leveduras, o que indiretamente prova que a produção de AAS é mais ecológica.
01 Desenvolvimento de aminoácidos
No início do século XIX, quando os aminoácidos que ocorrem naturalmente foram descobertos pela primeira vez, suas estruturas foram previstas como extremamente valiosas - utilizáveis como matérias -primas para a preparação de anfifiles. O primeiro estudo sobre a síntese de AAS foi relatado por Bondi em 1909.
Nesse estudo, a n-acilglicina e a n-acilalanina foram introduzidas como grupos hidrofílicos para surfactantes. O trabalho subsequente envolveu a síntese de lipoaminoácidos (AAs) usando glicina e alanina, e Hentrich et al. publicou uma série de descobertas,incluindo a primeira aplicação de patente, sobre o uso de sais de sarcosinato de acila e acil como surfactantes em produtos de limpeza doméstica (por exemplo, shampoos, detergentes e cremes dentais).Posteriormente, muitos pesquisadores investigaram a síntese e as propriedades físico -químicas dos aminoácidos acil. Até o momento, um grande corpo de literatura foi publicado sobre a síntese, propriedades, aplicações industriais e biodegradabilidade do AAS.
02 Propriedades estruturais
As cadeias de ácidos graxos hidrofóbicos não polares de AAS podem variar em estrutura, comprimento e número da cadeia.A diversidade estrutural e a alta atividade superficial dos AAs explicam sua ampla diversidade de composição e propriedades físico -químicas e biológicas. Os grupos de AAs são compostos de aminoácidos ou peptídeos. As diferenças nos grupos principais determinam a adsorção, agregação e atividade biológica desses surfactantes. Os grupos funcionais do grupo principal determinam o tipo de AAS, incluindo catiônicos, aniônicos, não iônicos e anfotéricos. A combinação de aminoácidos hidrofílicos e porções de cadeia longa hidrofóbica formam uma estrutura anfifílica que torna a molécula altamente superficial ativa. Além disso, a presença de átomos de carbono assimétrico na molécula ajuda a formar moléculas quirais.
03 Composição química
Todos os peptídeos e polipeptídeos são os produtos de polimerização desses quase 20 α-aminoácidos α-proteinogênicos. Todos os 20 α-aminoácidos contêm um grupo funcional do ácido carboxílico (-COOH) e um grupo funcional amino (-NH 2), ambos ligados ao mesmo átomo de α-carbono tetraédrico. Os aminoácidos diferem entre si pelos diferentes grupos R ligados ao α-carbono (exceto na licina, onde o grupo R é hidrogênio.) Os grupos R podem diferir em estrutura, tamanho e carga (acidez, alcalinidade). Essas diferenças também determinam a solubilidade dos aminoácidos na água.
Os aminoácidos são quirais (exceto a glicina) e são opticamente ativos por natureza porque têm quatro substituintes diferentes ligados ao carbono alfa. Os aminoácidos têm duas conformações possíveis; Eles são imagens de espelho que não sobrecarregam, apesar de o número de L-estteroisômeros ser significativamente mais altos. O grupo R presente em alguns aminoácidos (fenilalanina, tirosina e triptofano) é Aril, levando a uma absorção máxima de UV a 280 nm. O α-COOH ácido e o α-NH 2 básico em aminoácidos são capazes de ionização, e ambos os estereoisômeros, o que forem, construir o equilíbrio de ionização mostrado abaixo.
R-cooh ↔r-coo-+ h+
R-NH3+↔R-NH2+ h+
Como mostrado no equilíbrio de ionização acima, os aminoácidos contêm pelo menos dois grupos fracamente ácidos; No entanto, o grupo carboxil é muito mais ácido em comparação com o grupo amino protonado. PH 7,4, o grupo carboxila é desprotonado enquanto o grupo amino é protonado. Os aminoácidos com grupos R não ionizáveis são eletricamente neutros nesse pH e formam zwitterion.
04 Classificação
O AAS pode ser classificado de acordo com quatro critérios, que são descritos abaixo por sua vez.
4.1 De acordo com a origem
| De acordo com a origem, o AAS pode ser dividido em 2 categorias da seguinte maneira. ① Categoria natural Alguns compostos que ocorrem naturalmente contendo aminoácidos também têm a capacidade de reduzir a tensão superficial/interfacial, e outros até excedem a eficácia dos glicolipídios. Esses AAs também são conhecidos como lipopeptídeos. Os lipopeptídeos são compostos de baixo peso molecular, geralmente produzidos por espécies de Bacillus.
Tais AAs são divididos em 3 subclasses:surfactina, iturina e fengycina.
|
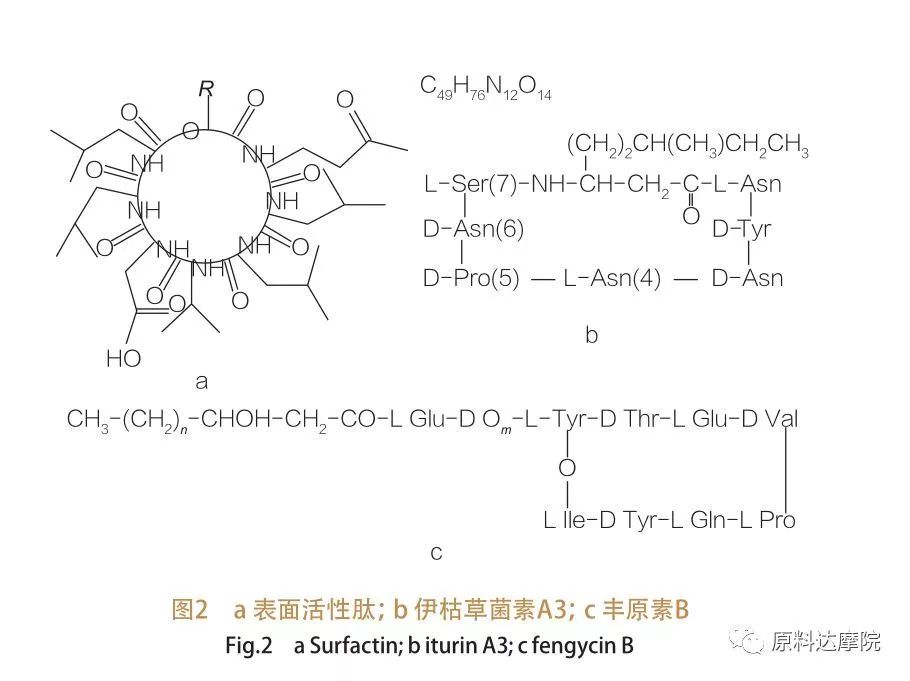
| A família de peptídeos de superfície ativa abrange variantes de heptapeptídeos de uma variedade de substâncias,como mostrado na Figura 2a, no qual uma cadeia de ácidos graxos β-hidroxi não saturada C12-C16 está ligada ao peptídeo. O peptídeo ativo na superfície é uma lactona macrocíclica na qual o anel é fechado por catálise entre o terminal C do ácido graxo β-hidroxi e o peptídeo. Na subclasse de Iturin, existem seis variantes principais, a saber, iterina A e C, micosubtilina e bacilomicina D, F e L.Em todos os casos, os heptapeptídeos estão ligados às cadeias C14-C17 dos ácidos graxos β-amino (as cadeias podem ser diversas). No caso das ekurimicinas, o grupo amino na posição β pode formar uma ligação amida com o terminal C, formando uma estrutura de lactama macrocíclica.
A subclasse fengycina contém fengycina A e B, que também são chamados de plipastatina quando o Tyr9 é configurado em D.O decapeptídeo está ligado a uma cadeia de ácidos graxos β -hidroxi saturada ou insaturada C14 -C18. Estruturalmente, a plipastatina também é uma lactona macrocíclica, contendo uma cadeia lateral Tyr na posição 3 da sequência peptídica e formando uma ligação éster com o resíduo C-terminal, formando uma estrutura interna do anel (como é o caso de muitos lipopeptídeos de Pseudomonas).
② Categoria sintética O AAS também pode ser sintetizado usando qualquer um dos aminoácidos ácido, básico e neutro. Os aminoácidos comuns utilizados para a síntese de AAs são ácido glutâmico, serina, prolina, ácido aspártico, glicina, arginina, alanina, leucina e hidrolisados de proteínas. Essa subclasse de surfactantes pode ser preparada por métodos químicos, enzimáticos e quimioenzimáticos; No entanto, para a produção de AAS, a síntese química é mais economicamente viável. Exemplos comuns incluem ácido n-lauroyl-l-glutâmico e ácido n-palmitoil-l-glutâmico.
|
4.2 com base em substituintes da cadeia alifática
Com base nos substituintes da cadeia alifática, os surfactantes à base de aminoácidos podem ser divididos em 2 tipos.
| Aas substituídas por N. Em compostos substituídos de N, um grupo amino é substituído por um grupo lipofílico ou um grupo carboxila, resultando em uma perda de basicidade. O exemplo mais simples dos AAs substituídos por N são os aminoácidos N-acil, que são essencialmente surfactantes aniônicos. Os AAs substituídos por N têm uma ligação amida anexada entre as porções hidrofóbicas e hidrofílicas. A ligação amida tem a capacidade de formar uma ligação de hidrogênio, que facilita a degradação desse surfactante em um ambiente ácido, tornando -a biodegradável.
②C AAS substituído por C. Nos compostos substituídos por C, a substituição ocorre no grupo carboxila (por meio de uma ligação amida ou éster). Os compostos típicos substituídos por C (por exemplo, ésteres ou amidas) são essencialmente surfactantes catiônicos.
AAs substituídos por C-e C e C Nesse tipo de surfactante, os grupos amino e carboxil são a parte hidrofílica. Este tipo é essencialmente um surfactante anfotérico. |
4.3 De acordo com o número de caudas hidrofóbicas
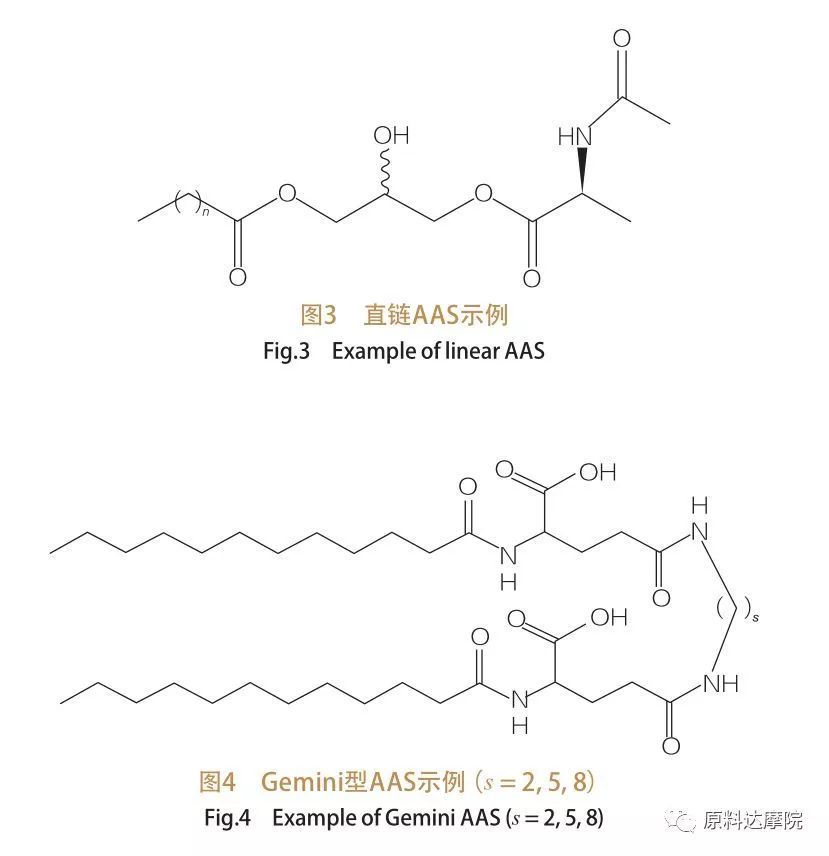
Com base no número de grupos principais e caudas hidrofóbicas, o AAS pode ser dividido em quatro grupos. AAS de cadeia reta, gêmeos (dímer) tipo AAs, glicerolipídios AAS e anfifílico bicefálico (BOLA) tipo AAS. Os surfactantes de cadeia reta são surfactantes que consistem em aminoácidos com apenas uma cauda hidrofóbica (Figura 3). Os gêmeos do tipo AAS têm dois grupos de cabeça polar de aminoácidos e duas caudas hidrofóbicas por molécula (Figura 4). Nesse tipo de estrutura, os dois AAs de cadeia reta são ligados por um espaçador e, portanto, também são chamados de dímeros. No tipo AAS glicerolipídico, por outro lado, as duas caudas hidrofóbicas são presas ao mesmo grupo de cabeça de aminoácidos. Esses surfactantes podem ser considerados análogos de monoglicerídeos, diglicerídeos e fosfolipídios, enquanto em AA do tipo Bola, dois grupos de cabeça de aminoácidos são ligados por uma cauda hidrofóbica.
4.4 De acordo com o tipo de grupo de cabeça
①Cationic AAS
O grupo principal desse tipo de surfactante tem uma carga positiva. O AAS catiônico mais antigo é o arginato de etilo Cocoyl, que é um carboxilato de pirrolidona. As propriedades únicas e diversas desse surfactante o tornam útil em desinfetantes, agentes antimicrobianos, agentes antistáticos, condicionadores de cabelo, além de serem suaves nos olhos e na pele e facilmente biodegradáveis. Singare e Mhatre sintetizaram AAs à base de arginina e avaliaram suas propriedades físico-químicas. Neste estudo, eles reivindicaram altos rendimentos dos produtos obtidos usando condições de reação de Schotten-Baumann. Com o aumento do comprimento da cadeia alquil e a hidrofobicidade, verificou -se que a atividade superficial do surfactante aumenta e a concentração crítica de micelas (CMC) diminui. Outro é a proteína acil quaternária, que é comumente usada como condicionador em produtos para cuidados capilares.
②aniionic AAS
Nos surfactantes aniônicos, o grupo principal polar do surfactante tem uma carga negativa. A sarcosina (CH 3 -NH -CH 2 -COOH, n -metilglicina), um aminoácido comumente encontrado em ouriços do mar e estrelas do mar, está quimicamente relacionado à glicina (NH 2 -Ch 2 -COOH), um aminoácido básico encontrado nas células mamíferas. -Cooh,) está quimicamente relacionado à glicina, que é um aminoácido básico encontrado nas células de mamíferos. O ácido láurico, o ácido tetradecanóico, o ácido oleico e seus halogenetos e ésteres são comumente usados para sintetizar surfactantes sarcosinados. Os sarcosinados são inerentemente leves e, portanto, são comumente usados em enxaguatórios bucais, xampus, espumas de barbear pulverizadas, filtros solares, limpadores de pele e outros produtos cosméticos.
Outros AAs aniônicos disponíveis comercialmente incluem o AMisoft CS-22 e o AmiliteGCK-12, que são nomes comerciais para N-co-l-L-glutamato e potássio glicinato de potássio, respectivamente. A amilita é comumente usada como agente de espuma, detergente, solubilizador, emulsificante e dispersante, e possui muitas aplicações em cosméticos, como xampus, sabonetes de banho, lavagens corporais, cremes dentais, limpadores faciais, sabonetes de limpeza, limpadores de lentes de contato e surfactantes domésticos. A Amisoft é usada como um limpador suave de pele e cabelo, principalmente em produtos de limpeza facial e corporal, detergentes sintéticos em bloqueio, produtos para cuidados com o corpo, xampus e outros produtos para cuidados com a pele.
③zwitteriônicos ou anfotéricos AAs
Os surfactantes anfotéricos contêm locais ácidos e básicos e, portanto, podem alterar sua carga alterando o valor do pH. Nos meios alcalinos, eles se comportam como surfactantes aniônicos, enquanto em ambientes ácidos se comportam como surfactantes catiônicos e em meios neutros como surfactantes anfotéricos. Lauril lisina (LL) e alcoxi (2-hidroxipropil) arginina são os únicos surfactantes anfotéricos conhecidos baseados em aminoácidos. LL é um produto de condensação de lisina e ácido láurico. Devido à sua estrutura anfotérica, LL é insolúvel em quase todos os tipos de solventes, exceto solventes muito alcalinos ou ácidos. Como pó orgânico, LL possui excelente adesão às superfícies hidrofílicas e um baixo coeficiente de atrito, dando a esse surfactante excelente capacidade de lubrificação. O LL é amplamente utilizado em cremes para a pele e condicionadores de cabelo e também é usado como lubrificante.
④noniionic AAS
Os surfactantes não iônicos são caracterizados por grupos polares sem acusações formais. Oito novos surfactantes não iônicos etoxilados foram preparados por al-Sabagh et al. de α-aminoácidos solúveis em óleo. Nesse processo, a L-fenilalanina (LEP) e a L-leucina foram esterificadas pela primeira vez com hexadecanol, seguidas de meio com ácido palmítico para dar duas amidas e dois ésteres de α-aminoácidos. As amidas e os ésteres foram submetidos a reações de condensação com óxido de etileno para preparar três derivados de fenilalanina com diferentes números de unidades de polioxietileno (40, 60 e 100). Essas AAs não iiônicas tiveram boas propriedades de detergência e espuma.
05 Síntese
5.1 Rota sintética básica
Na AAS, os grupos hidrofóbicos podem ser ligados a locais de amina ou ácido carboxílico ou através das cadeias laterais de aminoácidos. Com base nisso, quatro rotas sintéticas básicas estão disponíveis, conforme mostrado na Figura 5.
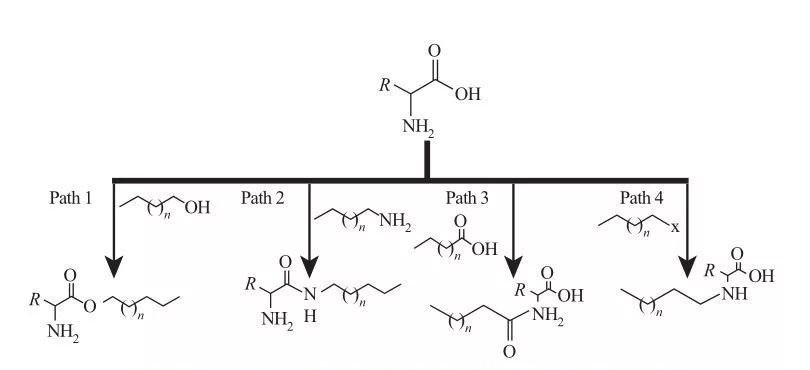
Fig.5 Caminhos de síntese fundamental de surfactantes à base de aminoácidos
| Caminho 1. As aminas do éster anfifílico são produzidas por reações de esterificação; nesse caso, a síntese de surfactante é geralmente alcançada por refluxo com álcoois graxos e aminoácidos na presença de um agente desidratante e um catalisador ácido. Em algumas reações, o ácido sulfúrico atua como um catalisador e um agente desidratante.
Caminho 2. Os aminoácidos ativados reagem com alquilaminas para formar ligações amidas, resultando na síntese de amidoaminas anfifílicas.
Caminho 3. Os ácidos amido são sintetizados reagindo os grupos de amina de aminoácidos com ácidos amido.
Caminho 4. Os aminoácidos de alquil de cadeia longa foram sintetizados pela reação de grupos de amina com haloalquanos. |
5.2 Avanços na síntese e produção
5.2.1 Síntese de aminoácidos de cadeia única/surfactantes peptídicos
Os aminoácidos ou peptídeos n-acil ou O-acil podem ser sintetizados por acilação catalisada por enzimas de grupos de amina ou hidroxila com ácidos graxos. O relatório mais antigo sobre a síntese catalisada por lipase livre de solvente de derivados de aminoácidos aminoácidos ou éster metil usou Candida Antarctica, com rendimentos variando de 25% a 90%, dependendo do aminoácido alvo. A metil etil cetona também tem sido usada como solvente em algumas reações. Vonderhagen et al. Também descreveram as reações de n-acilação de lipase e catalisadas por aminoácidos, hidrolisados de proteínas e/ou seus derivados usando uma mistura de água e solventes orgânicos (por exemplo, dimetilformamida/água) e metil butil-cetona.
Nos primeiros dias, o principal problema com a síntese de AAs catalisada por enzimas eram os baixos rendimentos. De acordo com Valivety et al. O rendimento dos derivados de aminoácidos N-tetradecanoil foi de apenas 2% a 10%, mesmo após o uso de lipases diferentes e incubando a 70 ° C por muitos dias. Montet et al. Também encontrou problemas relativos ao baixo rendimento de aminoácidos na síntese de lisina N-acil usando ácidos graxos e óleos vegetais. Segundo eles, o rendimento máximo do produto foi de 19% em condições livres de solvente e usando solventes orgânicos. O mesmo problema foi encontrado por Valivety et al. na síntese de derivados de éster metil-lisina N-CBZ-L-lisina ou N-CBZ-lisina.
Neste estudo, eles alegaram que o rendimento de 3-O-Tetradecanoil-L-Serina era de 80% ao usar a serina protegida por N como substrato e Novozyme 435 como catalisador em um ambiente livre de solvente fundido. Nagao and Kito studied the O-acylation of L-serine, L-homoserine, L-threonine and L-tyrosine (LET) when using lipase The results of the reaction (lipase was obtained by Candida cylindracea and Rhizopus delemar in aqueous buffer medium) and reported that the yields of acylation of L-homoserine and L-serine were somewhat low, while no acilação da L-Treonina e deixou ocorrer.
Muitos pesquisadores apoiaram o uso de substratos baratos e prontamente disponíveis para a síntese de AAs econômicos. Soo et al. alegou que a preparação de surfactantes à base de óleo de palma funciona melhor com lipoenzima imobilizada. Eles observaram que o rendimento dos produtos seria melhor, apesar da reação demorada (6 dias). Gerova et al. investigou a síntese e a atividade da superfície do N-Palmitoil AAS, baseado em metionina, prolina, leucina, treonina, fenilalanina e fenilglicina em uma mistura cíclica/racêmica. Pang e Chu descreveram a síntese de monômeros à base de aminoácidos e monômeros à base de ácido dicarboxílico em solução Uma série de ésteres de poliamida baseados em aminoácidos funcionais e biodegradáveis foram sintetizados por reações de co-recomenda em solução.
Canteuzeno e Guerreiro relataram a esterificação de grupos de ácido carboxílico de BOC-ALA-OH e BOC-ASP-OH com álcoois e dióis alifáticos de cadeia longa, com diclorometano como solvente e agarose 4b (Sepharose 4b) como catalisador. Neste estudo, a reação do BOC-ALA-OH com álcoois gordurosos de até 16 carbonos deu bons rendimentos (51%), enquanto para BOC-ASP-OH 6 e 12 carbonos foram melhores, com um rendimento correspondente de 63% [64]. 99,9%) em rendimentos variando de 58%a 76%, que foram sintetizados pela formação de ligações amidas com várias alquilaminas de cadeia longa ou ligações éster com álcoois graxos por CBZ-ARG-AME, onde a papaína atuava como catalisador.
5.2.2 Síntese de surfactantes de aminoácidos/peptídeos à base de Gêmeos
Os surfactantes de gêmeos à base de aminoácidos consistem em duas moléculas de AAS de cadeia reta vinculadas entre si por um grupo espaçador. Existem 2 esquemas possíveis para a síntese quimioenzimática de surfactantes à base de aminoácidos do tipo gêmeos (Figuras 6 e 7). Na Figura 6, 2 derivados de aminoácidos são reagidos com o composto como um grupo espaçador e, em seguida, são introduzidos 2 grupos hidrofóbicos. Na Figura 7, as 2 estruturas de cadeia reta são diretamente ligadas por um grupo espaçador bifuncional.
O desenvolvimento mais antigo da síntese catalisada por enzimas de lipoaminoácidos de Gêmeos foi pioneira por Valivety et al. Yoshimura et al. investigaram a síntese, adsorção e agregação de um surfactante de gêmeos à base de aminoácidos baseado em cistina e brometo de N-alquil. Os surfactantes sintetizados foram comparados com os surfactantes monoméricos correspondentes. Faustino et al. descreveram a síntese de AA monomérico à base de uréia aniônica, baseada em L-cistina, D-cistina, DL-cistina, L-cisteína, L-metionina e L-sulfoalanina e seus pares de gêmeos por meio de condutividade, equilíbrio tensão da superfície da superfície e a caracterização de fluorescência do estado. Foi demonstrado que o valor CMC de Gêmeos foi menor comparando monômero e gêmeos.
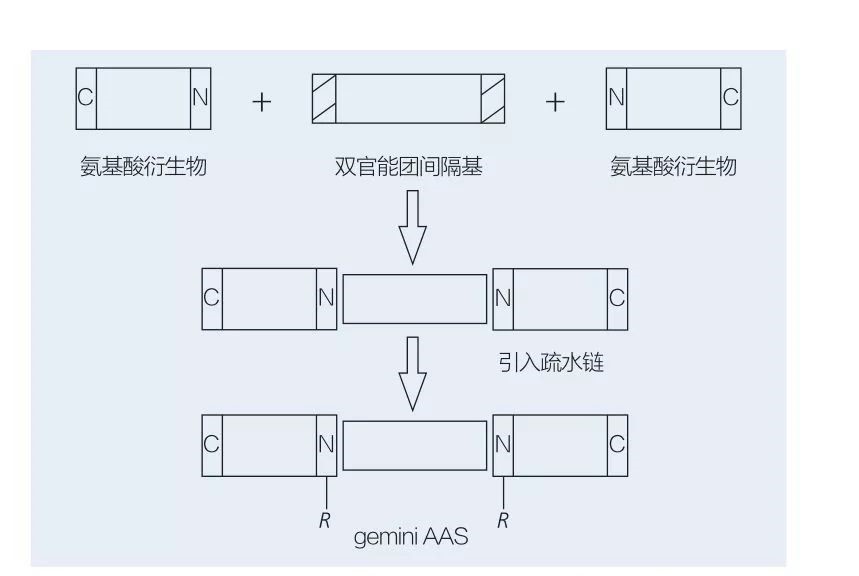
Fig.6 Síntese de Gêmeos AAs usando derivados AA e espaçador, seguido pela inserção do grupo hidrofóbico
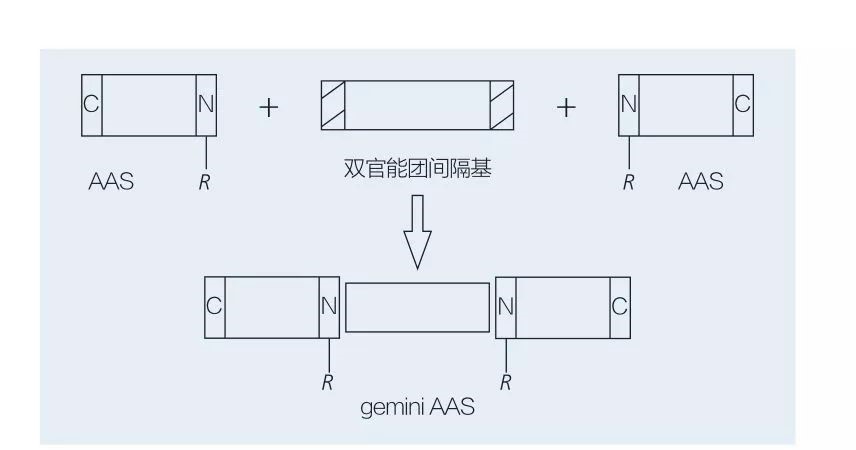
Fig.7 Síntese de Gêmeos Aass usando espaçador bifuncional e AAS
5.2.3 Síntese de aminoácidos glicerolipídicos/surfactantes peptídicos
Os surfactantes de aminoácidos/peptídeos glicerolipídios são uma nova classe de aminoácidos lipídicos que são análogos estruturais de ésteres e fosfolipídios mono- (ou di-) de glicerol, devido à sua estrutura de uma ou duas cadeias gordurosas com um aminoácido ligado ao bico de glicerol por um vínculo de ESTER. A síntese desses surfactantes começa com a preparação de ésteres de glicerol de aminoácidos a temperaturas elevadas e na presença de um catalisador ácido (por exemplo, BF 3). A síntese catalisada por enzimas (usando hidrolases, proteases e lipases como catalisadores) também é uma boa opção (Figura 8).
Foi relatado que a síntese catalisada por enzimas de conjugados de glicerídeos arginina diláuridos usando papaína foi relatada. Também foram relatados síntese de conjugados de éster de diacilglicerol da acetilarginina e a avaliação de suas propriedades físico -químicas.
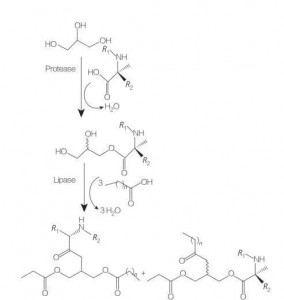
Fig.8 Síntese de conjugados de aminoácidos mono e diacilglicerol
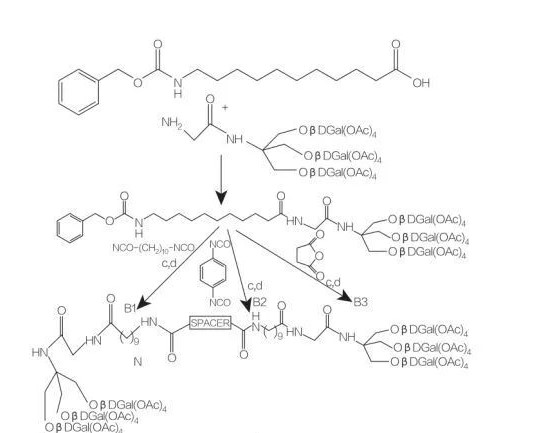
Spacer: NH- (cap2)10-Nh: compostob1
Spacer: NH-C6H4-Nh: compostob2
espaçador: cap2-Ch2
Fig.9 Síntese de anfifilos simétricos derivados de Tris (hidroximetil) aminometano
5.2.4 Síntese de surfactantes de aminoácidos/peptídeos à base de BOLA/peptídeos
Os anfifiles do tipo Bola à base de aminoácidos contêm 2 aminoácidos que estão ligados à mesma cadeia hidrofóbica. Franceschi et al. descreveram a síntese de anfifilos do tipo BOLA com 2 aminoácidos (D- ou L-alanina ou L-histidina) e 1 cadeia alquil de diferentes comprimentos e investigaram sua atividade superficial. Eles discutem a síntese e agregação de novos anfifiles do tipo Bola com uma fração de aminoácidos (usando um β-aminoácido incomum ou um álcool) e um grupo espaçador C12-C20. Os β-aminoácidos incomuns utilizados podem ser um aminoácido de açúcar, um aminoácido derivado de azidotimina (AZT), um aminoácido norborborno e um álcool amino derivado do AZT (Figura 9). A síntese de anfífilos simétricos do tipo Bola derivados de Tris (hidroximetil) aminometano (Tris) (Figura 9).
06 Propriedades físico -químicas
É sabido que os surfactantes à base de aminoácidos (AAs) são diversos e versáteis de natureza e têm boa aplicabilidade em muitas aplicações, como boa solubilização, boas propriedades de emulsificação, alta eficiência, alto desempenho da atividade superficial e boa resistência à água dura (tolerância ao íons de cálcio).
Com base nas propriedades do surfactante dos aminoácidos (por exemplo, tensão superficial, CMC, comportamento de fase e temperatura de Krafft), as seguintes conclusões foram alcançadas após estudos extensos - a atividade superficial do AAS é superior à de sua contraparte de surfactante convencional.
6.1 Concentração crítica de micelas (CMC)
A concentração crítica de micelas é um dos parâmetros importantes dos surfactantes e governa muitas propriedades ativas da superfície, como solubilização, lise celular e sua interação com biofilmes, etc. Em geral, aumentando o comprimento da cadeia da cauda de hidrocarbono (aumento da hidrofobicidade) leva a uma diminuição no valor do CMC da solução de surfação, assim o aumento da atividade. Os surfactantes baseados em aminoácidos geralmente apresentam valores mais baixos de CMC em comparação aos surfactantes convencionais.
Através de diferentes combinações de grupos de cabeça e caudas hidrofóbicas (amida monocatória, amida bi-cacionica, éster bi-cacionalidade à base de amida), Infante et al. sintetizou três AA à base de arginina e estudou seu CMC e γCMC (tensão superficial no CMC), mostrando que os valores de CMC e γCMC diminuíram com o aumento do comprimento da cauda hidrofóbica. Em outro estudo, Singare e Mhatre descobriram que o CMC de surfactantes de N-α-aclarginina diminuiu com o aumento do número de átomos de carbono de cauda hidrofóbica (Tabela 1).
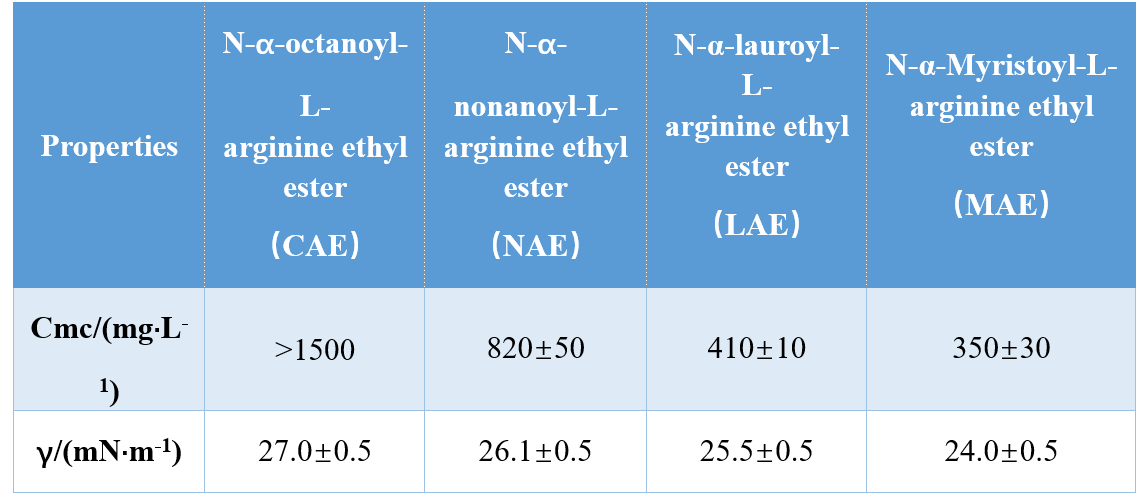
Yoshimura et al. Investigou o CMC de surfactantes de gêmeos à base de aminoácidos derivados da cisteína e mostraram que o CMC diminuiu quando o comprimento da cadeia de carbono na cadeia hidrofóbica aumentou de 10 para 12. O aumento do comprimento da cadeia de carbono para 14 resultou em um aumento no CMC, o que confirmou que os surfactantes de gêmeos de cadeia longa têm uma tendência menor a agrogem.
Faustino et al. relataram a formação de micelas mistas em soluções aquosas de surfactantes aniônicos de Gêmeos com base na cistina. Os surfactantes de Gêmeos também foram comparados com os surfactantes monoméricos convencionais correspondentes (C 8 Cys). Os valores de CMC das misturas lipídicas surfactantes foram relatadas como menores do que os de surfactantes puros. Os surfactantes de gêmeos e 1,2-diheptonoil-sn-gliceril-3-fosfocolina, um fosfolipídeo que solúvel em água solúvel em micela, teve CMC no nível milimolar.
Shrestha e Aamaki investigaram a formação de micelas viscoelásticas do tipo verme em soluções aquosas de surfactantes aniônicos-não-noniônicos à base de aminoácidos misturados na ausência de sais de mistura. Neste estudo, verificou-se que o glutamato de N-Dodecil possui uma temperatura mais alta de Krafft; No entanto, quando neutralizado com o aminoácido básico L-lisina, gerou micelas e a solução começou a se comportar como um fluido newtoniano a 25 ° C.
6.2 Boa solubilidade em água
A boa solubilidade em água do AAS se deve à presença de ligações co-NH adicionais. Isso torna o AAS mais biodegradável e ecológico do que os surfactantes convencionais correspondentes. A solubilidade da água do ácido n-acil-L-glutâmico é ainda melhor devido aos seus 2 grupos carboxila. A solubilidade da água do CN (CA) 2 também é boa porque existem 2 grupos argininos iônicos em 1 molécula, o que resulta em adsorção e difusão mais eficazes na interface celular e até inibição bacteriana eficaz em concentrações mais baixas.
6.3 Temperatura de Krafft e Ponto Krafft
A temperatura de Krafft pode ser entendida como o comportamento específico da solubilidade dos surfactantes cuja solubilidade aumenta acentuadamente acima de uma temperatura específica. Os surfactantes iônicos tendem a gerar hidratos sólidos, que podem precipitar fora da água. Em uma temperatura específica (a chamada temperatura de Krafft), geralmente é observado um aumento dramático e descontínuo na solubilidade dos surfactantes. O ponto de Krafft de um surfactante iônico é sua temperatura de Krafft no CMC.
Essa característica de solubilidade é geralmente vista para surfactantes iônicos e pode ser explicada da seguinte forma: a solubilidade do monômero livre de surfactante está limitada abaixo da temperatura de Krafft até que o ponto de Krafft seja atingido, onde sua solubilidade aumenta gradualmente devido à formação de micelas. Para garantir a solubilidade completa, é necessário preparar formulações de surfactantes a temperaturas acima do ponto de Krafft.
A temperatura de Krafft de AAs foi estudada e comparada com a dos surfactantes sintéticos convencionais. A Shrestha e a Aramaki estudaram a temperatura de Krafft da AAS à base de arginina e descobriu que a concentração crítica de micelas exibia comportamento de agregação da forma de Micelles acima de 2-5 × 10-6 Mol-L-L-L-L-L-Syngeation (OHTE de Micelle (OHTE ETL ETAT. discutiu a relação entre a temperatura de Krafft e os resíduos de aminoácidos.
Nos experimentos, verificou-se que a temperatura de Krafft do N-hexadecanoil AAS aumentou com o tamanho decrescente dos resíduos de aminoácidos (sendo a fenilalanina uma exceção), enquanto o calor da solubilidade (captação de calor) aumentou com o tamanho decrescente dos resíduos de aminoácidos (com exceção da glicina e da fenilalanina). Concluiu-se que nos sistemas de alanina e fenilalanina, a interação DL é mais forte que a interação LL na forma sólida do sal n-hexadecanoil AAS.
Brito et al. Determinou a temperatura de Krafft de três séries de novos surfactantes à base de aminoácidos usando microcalorimetria de varredura diferencial e descobriu que a mudança do íon trifluoroacetato para o íons iodeto resultou em um aumento significativo na temperatura de Krafft (cerca de 6 ° C), de 47 ° C a 53 ° C. A presença de ligações cis duplas e a insaturação presente nos Ser-derivados de cadeia longa levaram a uma diminuição significativa na temperatura de Krafft. Foi relatado que o glutamato de N-Dodecil possui uma temperatura mais alta de Krafft. No entanto, a neutralização com o aminoácido básico L-lisina resultou na formação de micelas em solução que se comportou como fluidos newtonianos a 25 ° C.
6.4 Tensão superficial
A tensão superficial dos surfactantes está relacionada ao comprimento da cadeia da parte hidrofóbica. Zhang et al. Determinou a tensão superficial do glicinato de coco -coco de sódio pelo método da placa de Wilhelmy (25 ± 0,2) ° C e determinou o valor da tensão da superfície em CMC como 33 mn -m -1, cmc como 0,21 mmol -l -1. Yoshimura et al. determinou a tensão superficial do tipo de superfície de 2C N Cys baseado em aminoácidos, baseada na superfície de agentes ativos de superfície baseados em 2C N Cys. Verificou -se que a tensão superficial no CMC diminuiu com o aumento do comprimento da cadeia (até n = 8), enquanto a tendência foi revertida para surfactantes com n = 12 ou mais comprimentos de cadeia.
Também foi estudado o efeito do CAC1 2 na tensão superficial de surfactantes à base de aminoácidos dicarboxilados. Nesses estudos, o CAC1 2 foi adicionado a soluções aquosas de três surfactantes do tipo dicarboxilado (C12 Malna 2, C12 Aspna 2 e C12 Gluna 2). Os valores do platô após o CMC foram comparados e verificou -se que a tensão superficial diminuiu em concentrações muito baixas de CAC1 2. Isso se deve ao efeito dos íons cálcio no arranjo do surfactante na interface da água a gás. As tensões superficiais dos sais de N-dodecilaminomalonato e N-dodecilaspartato, por outro lado, também eram quase constantes até 10 mmol-l -1 Cac1 2. Acima de 10 mmol -l -1, a tensão superficial aumenta acentuadamente, devido à formação de uma precipitação do sal de cálcio do surfactante. Para o sal dissódico do glutamato N-dodecil, a adição moderada de CAC1 2 resultou em uma diminuição significativa na tensão superficial, enquanto o aumento contínuo da concentração de CAC1 2 não causou mais alterações significativas.
Para determinar a cinética de adsorção do AAS do tipo geminiano na interface da água a gás, a tensão dinâmica da superfície foi determinada usando o método máximo de pressão da bolha. Os resultados mostraram que, pelo tempo de teste mais longo, a tensão dinâmica da superfície 2C 12 Cys não mudou. A diminuição da tensão dinâmica da superfície depende apenas da concentração, do comprimento das caudas hidrofóbicas e do número de caudas hidrofóbicas. O aumento da concentração de surfactante, diminuindo o comprimento da cadeia e o número de cadeias resultou em uma deterioração mais rápida. Os resultados obtidos para concentrações mais altas de C N Cys (n = 8 a 12) foram muito próximas do γ CMC medido pelo método Wilhelmy.
Em outro estudo, as tensões dinâmicas da superfície da cistina dilauril de sódio (SDLC) e didecamino cistina de sódio foram determinadas pelo método da placa de Wilhelmy e, além disso, as tensões da superfície de equilíbrio de suas soluções aquosas foram determinadas pelo método do volume de queda. A reação das ligações dissulfeto também foi investigada por outros métodos. A adição de mercaptoetanol a uma solução 0,1 mmol -l -1SDLC levou a um rápido aumento na tensão superficial de 34 mn -m -1 a 53 Mn -M -1. Como o NACLO pode oxidar as ligações dissulfeto de SDLC em grupos de ácido sulfônico, não foram observados agregados quando o NACLO (5 mmol -l -1) foi adicionado à solução de 0,1 mmol -l -1 SDLC. Microscopia eletrônica de transmissão e resultados dinâmicos de espalhamento de luz mostraram que nenhum agregado foi formado na solução. Verificou -se que a tensão superficial do SDLC aumentou de 34 Mn -M -1 para 60 Mn -M -1 durante um período de 20 min.
6.5 Interações de superfície binária
Nas ciências da vida, vários grupos estudaram as propriedades vibracionais das misturas de AAs catiônicos (surfactantes à base de arginina de diacilglicerol) e fosfolipídios na interface da água a gás, finalmente concluindo que essa propriedade não ideal causa a prevalência de interações eletrostáticas.
6.6 Propriedades de agregação
A dispersão dinâmica da luz é comumente usada para determinar as propriedades de agregação de monômeros e surfactantes de gêmeos à base de aminoácidos em concentrações acima do CMC, produzindo um aparente diâmetro hidrodinâmico DH (= 2R H). Os agregados formados por C N Cys e 2CN Cys são relativamente grandes e têm uma distribuição em larga escala em comparação com outros surfactantes. Todos os surfactantes, exceto 2C 12, formam agregados de cerca de 10 nm. Os tamanhos de micelas dos surfactantes de gêmeos são significativamente maiores que os de seus colegas monoméricos. Um aumento no comprimento da cadeia de hidrocarbonetos também leva a um aumento no tamanho de micelas. Ohta et al. descreveram as propriedades de agregação de três diferentes estereoisômeros de N-Dodecil-fenil-alanil-fenil-alanina tetrametilamônio em solução aquosa e mostraram que os diateroisômeros têm a mesma concentração de agregação crítica em solução aquosa. Iwahashi et al. investigated by circular dichroism, NMR and vapor pressure osmometry the The formation of chiral aggregates of N-dodecanoyl-L-glutamic acid, N-dodecanoyl-L-valine and their methyl esters in different solvents (such as tetrahydrofuran, acetonitrile, 1,4-dioxane and 1,2-dichloroethane) with rotational properties was investigated by Dicroísmo circular, RMN e osmometria de pressão de vapor.
6.7 Adsorção interfacial
A adsorção interfacial de surfactantes à base de aminoácidos e sua comparação com sua contraparte convencional também é uma das direções da pesquisa. Por exemplo, foram investigadas as propriedades de adsorção interfacial dos ésteres de dodecil de aminoácidos aromáticos obtidos de LET e LEP. Os resultados mostraram que o LET e o LEP exibiram áreas interfaciais mais baixas na interface gás-líquido e na interface água/hexano, respectivamente.
Bordes et al. investigaram o comportamento da solução e a adsorção na interface de água a gás de três surfactantes de aminoácidos dicarboxilados, os sais de dissódio de dodecil glutamato, aspartato de dodecil e aminomalonato (com 3, 2 e 1 átomos de carbono entre os dois grupos carboxil, respectivamente). De acordo com este relatório, o CMC dos surfactantes dicarboxilados foi 4-5 vezes maior que o do sal de dodecil glicina monocarboxilado. Isso é atribuído à formação de ligações de hidrogênio entre os surfactantes dicarboxilados e as moléculas vizinhas através dos grupos amidas nele.
6.8 comportamento de fase
Fases cúbicas descontínicas isotrópicas são observadas para surfactantes em concentrações muito altas. Moléculas de surfactante com grupos de cabeça muito grandes tendem a formar agregados de curvatura positiva menor. Marques et al. Estudou o comportamento de fase dos sistemas 12LYS12/12Ser e 8LYS8/16Ser (veja a Figura 10), e os resultados mostraram que o sistema 12LYS12/12Ser possui uma zona de separação de fases entre as regiões da fase micelar e vesicular, enquanto o sistema de fase 8LONS8 e o sistema de fase de 8LOLS8/16SELOTS mostra uma transição contínua (o sistema de micloS8/16 anos e o sistema de micloS8/16 anos mostra uma contínua transição (o sistema Smalls8/16Ser, mostra uma transição contínua (o sistema de letra de fase 8LONS8/16SELS8/16SELOTS8/16SELONS, a fase de fase 8lys8/16Ser, a fase 8lys8/16Ser. região). Deve -se notar que, para a região da vesícula do sistema 12LYS12/12SER, as vesículas estão sempre coexistindo com micelas, enquanto a região da vesícula do sistema 8LYS8/16SER possui apenas vesículas.
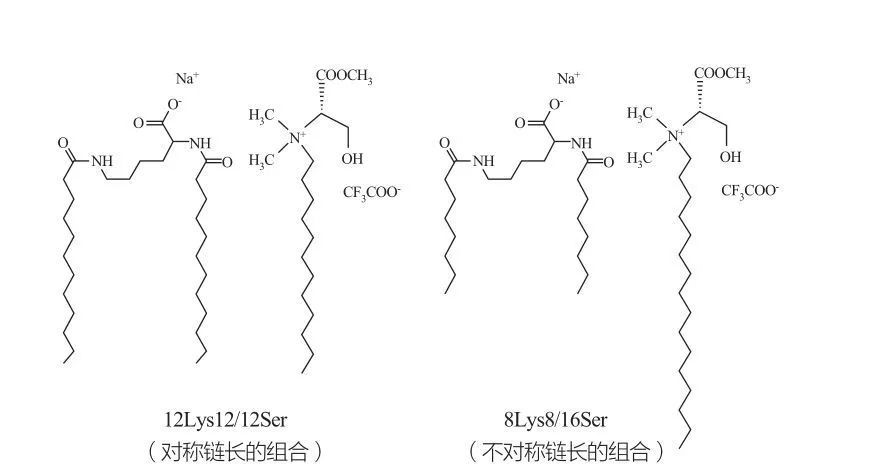
Misturas cataniônicas dos surfactantes à base de lisina e serina: par simétrico 12LYS12/12Ser (esquerda) e pares de 8lys8/16Ser assimétricos (à direita)
6.9 Habilidade emulsificante
Kouchi et al. examinou a capacidade emulsificante, a tensão interfacial, a dispersibilidade e a viscosidade de N- [3-dodecil-2-hidroxipropil] -l-arginina, L-glutamato e outros AAs. Em comparação com surfactantes sintéticos (seus colegas não iônicos e anfotéricos convencionais), os resultados mostraram que os AAs têm uma capacidade emulsificante mais forte que os surfactantes convencionais.
Baczko et al. Surfactantes de aminoácidos aniônicos sintetizados e investigaram sua adequação como solventes de espectroscopia de RMN orientados a quirais. Uma série de derivados anfifílicos L-Phe ou L-ALA à base de sulfonato com diferentes caudas hidrofóbicas (pentil ~ tetradecil) foram sintetizadas por reagir aminoácidos com an-hidreto O-Sulfobenzóico. Wu et al. sais de sódio sintetizados de acil AAs de gordura einvestigaram sua capacidade de emulsificação em emulsões petrolíferas em água, e os resultados mostraram que esses surfactantes tiveram melhor desempenho com acetato de etila como fase oleosa do que com n-hexano como fase oleosa.
6.10 Avanços na síntese e produção
A resistência à água dura pode ser entendida como a capacidade dos surfactantes de resistir à presença de íons como cálcio e magnésio em água dura, ou seja, a capacidade de evitar a precipitação nos sabonetes de cálcio. Os surfactantes com alta resistência à água dura são muito úteis para formulações de detergentes e produtos de cuidados pessoais. A resistência à água dura pode ser avaliada calculando a mudança na solubilidade e a atividade superficial do surfactante na presença de íons cálcio.
Outra maneira de avaliar a resistência à água dura é calcular a porcentagem ou gramas de surfactante necessários para o sabão de cálcio formado a partir de 100 g de oleato de sódio a ser disperso em água. Em áreas com alta água dura, altas concentrações de íons de cálcio e magnésio e conteúdo mineral podem dificultar as aplicações práticas. Freqüentemente, o íon de sódio é usado como o contractante de um surfactante aniônico sintético. Como o íon de cálcio divalente está ligado às duas moléculas de surfactante, faz com que o surfactante precipite mais facilmente a partir da solução, tornando a detergência menos provável.
O estudo da resistência à água dura do AAS mostrou que a resistência ao ácido e da água dura foi fortemente influenciada por um grupo carboxil adicional, e a resistência ao ácido e da água dura aumentou ainda mais com o aumento do comprimento do grupo espaçador entre os dois grupos carboxila. A ordem de resistência ao ácido e da água dura foi c 12 glicinato <c 12 aspartato <c 12 glutamato. Comparando a ligação amida dicarboxilada e o surfactante amino dicarboxilado, respectivamente, verificou -se que a faixa de pH do último era mais ampla e sua atividade superficial aumentou com a adição de uma quantidade apropriada de ácido. Os aminoácidos N-alquil dicarboxilados mostraram efeito quelante na presença de íons de cálcio e C 12 Gel branco formado em aspartato. C 12 O glutamato mostrou alta atividade superficial em alta concentração de Ca 2+ e deve ser usada na dessalinização da água do mar.
6.11 Dispersibilidade
Dispersibilidade refere -se à capacidade de um surfactante para prevenir a coalescência e sedimentação do surfactante em solução.A dispersibilidade é uma propriedade importante dos surfactantes que os torna adequados para uso em detergentes, cosméticos e produtos farmacêuticos.Um agente dispersor deve conter uma ligação éster, éter, amida ou amino entre o grupo hidrofóbico e o grupo hidrofílico terminal (ou entre os grupos hidrofóbicos da cadeia reta).
Geralmente, surfactantes aniônicos, como sulfatos de alcanolamido, e surfactantes anfotéricos, como amidosulfobetaína, são particularmente eficazes como agentes de dispersão para sabonetes de cálcio.
Muitos esforços de pesquisa determinaram a dispersibilidade do AAS, onde a n-lauroyl lisina foi mal compatível com a água e difícil de usar para formulações cosméticas.Nesta série, os aminoácidos básicos substituídos por N-acil têm excelente dispersibilidade e são usados na indústria cosmética para melhorar as formulações.
07 Toxicidade
Os surfactantes convencionais, especialmente os surfactantes catiônicos, são altamente tóxicos para os organismos aquáticos. Sua toxicidade aguda se deve ao fenômeno da interação de íons de adsorção de surfactantes na interface celular. A diminuição do CMC dos surfactantes geralmente leva a uma adsorção interfacial mais forte de surfactantes, o que geralmente resulta em sua toxicidade aguda elevada. Um aumento no comprimento da cadeia hidrofóbica de surfactantes também leva a um aumento na toxicidade aguda do surfactante.A maioria dos AAs é baixa ou não tóxica para os seres humanos e o meio ambiente (especialmente para organismos marinhos) e é adequado para uso como ingredientes alimentares, produtos farmacêuticos e cosméticos.Muitos pesquisadores demonstraram que os surfactantes de aminoácidos são gentis e não irritórios para a pele. Sabe-se que os surfactantes à base de arginina são menos tóxicos do que seus colegas convencionais.
Brito et al. estudaram as propriedades físico-químicas e toxicológicas dos anfifiles à base de aminoácidos e seus [derivados da tirosina (Tyr), hidroxiprolina (HYP), serina (Ser) e lisina (Lys)] Formação Espontânea de Vesículas Catiais e deu dados sobre a toxicidade escolar e dáforo. Eles sintetizaram vesículas catiônicas de brometo de dodeciltrimetilamônio (DTAB)/derivados e/ou misturas derivadas de Ser/Lys e testaram sua ecotoxicidade e potencial hemolítico, mostrando que todas as misturas de AAs e suas misturas contendo vesículas foram menos toxic do que o intervalo convencional.
Rosa et al. investigou a ligação (associação) do DNA a vesículas catiônicas estáveis à base de aminoácidos. Ao contrário dos surfactantes catiônicos convencionais, que geralmente parecem ser tóxicos, a interação de surfactantes de aminoácidos catiônicos parece não ser tóxica. O AAS catiônico é baseado na arginina, que forma espontaneamente vesículas estáveis em combinação com certos surfactantes aniônicos. Os inibidores de corrosão à base de aminoácidos também são relatados como não tóxicos. Esses surfactantes são facilmente sintetizados com alta pureza (até 99%), baixo custo, facilmente biodegradável e completamente solúvel em meios aquosos. Vários estudos mostraram que os surfactantes de aminoácidos contendo enxofre são superiores na inibição da corrosão.
Em um estudo recente, Perinelli et al. relataram um perfil toxicológico satisfatório dos ramnolipídios em comparação com os surfactantes convencionais. Sabe -se que os ramnolipídios atuam como intensificadores de permeabilidade. Eles também relataram o efeito dos ramnolipídios na permeabilidade epitelial dos medicamentos macromoleculares.
08 Atividade antimicrobiana
A atividade antimicrobiana dos surfactantes pode ser avaliada pela concentração inibitória mínima. A atividade antimicrobiana dos surfactantes à base de arginina foi estudada em detalhes. Verificou-se que as bactérias gram-negativas eram mais resistentes a surfactantes à base de arginina do que as bactérias gram-positivas. A atividade antimicrobiana dos surfactantes geralmente é aumentada pela presença de hidroxil, ciclopropano ou ligações insaturadas nas cadeias acil. Castillo et al. mostraram que o comprimento das cadeias acil e a carga positiva determinam o valor do HLB (equilíbrio hidrofílico-lipofílico) da molécula, e estes afetam sua capacidade de interromper as membranas. O éster metil nα-aclarginina é outra classe importante de surfactantes catiônicos com atividade antimicrobiana de amplo espectro e é facilmente biodegradável e tem baixa ou sem toxicidade. Studies on the interaction of Nα-acylarginine methyl ester-based surfactants with 1,2-dipalmitoyl-sn-propyltrioxyl-3-phosphorylcholine and 1,2-ditetradecanoyl-sn-propyltrioxyl-3-phosphorylcholine, model membranes, and with living organisms in the presence or absence of external barriers have shown that this class of surfactants has good Antimicrobiano Os resultados mostraram que os surfactantes têm boa atividade antibacteriana.
09 Propriedades reológicas
As propriedades reológicas dos surfactantes desempenham um papel muito importante na determinação e previsão de suas aplicações em diferentes indústrias, incluindo alimentos, produtos farmacêuticos, extração de petróleo, cuidados pessoais e produtos para cuidados domiciliares. Muitos estudos foram realizados para discutir a relação entre viscoelasticidade dos surfactantes de aminoácidos e CMC.
10 aplicações na indústria cosmética
Os AAs são usados na formulação de muitos produtos de cuidados pessoais.Verificou-se que o glicinato de potássio N-cocoil é suave na pele e é usado na limpeza facial para remover o lodo e a maquiagem. O ácido n-acil-L-glutâmico possui dois grupos carboxila, o que o torna mais solúvel em água. Entre esses AAs, os AAs baseados em ácidos graxos C 12 são amplamente utilizados na limpeza facial para remover o lodo e a maquiagem. AAs com uma cadeia C 18 são usados como emulsificantes em produtos para cuidados com a pele, e os sais de alanina n-lauryl são conhecidos por criar espumas cremosas que não são irritantes para a pele e, portanto, podem ser usadas na formulação de produtos para cuidados com o bebê. Os AA baseados em n-lauryl usados em pasta de dente têm boa detergência semelhante ao sabão e forte eficácia inibindo a enzima.
Nas últimas décadas, a escolha de surfactantes para cosméticos, produtos de cuidados pessoais e produtos farmacêuticos se concentrou em baixa toxicidade, brandura, gentileza com o toque e a segurança. Os consumidores desses produtos estão cientes da potencial irritação, toxicidade e fatores ambientais.
Hoje, os AAs são usados para formular muitos xampus, corantes capilares e sabonetes de banho devido a suas muitas vantagens sobre seus colegas tradicionais em cosméticos e produtos de cuidados pessoais.Os surfactantes à base de proteínas têm propriedades desejáveis necessárias para produtos de cuidados pessoais. Alguns AAs têm recursos de formação de filmes, enquanto outros têm boas capacidades de espuma.
Os aminoácidos são importantes fatores hidratantes que ocorrem naturalmente no estrato córneo. Quando as células epidérmicas morrem, elas se tornam parte do estrato córneo e as proteínas intracelulares são gradualmente degradadas em aminoácidos. Esses aminoácidos são então transportados ainda mais para o estrato córneo, onde absorvem substâncias de gordura ou gordura no estrato epidérmico córneo, melhorando assim a elasticidade da superfície da pele. Aproximadamente 50% do fator hidratante natural na pele é composto de aminoácidos e pirrolidona.
O colágeno, um ingrediente cosmético comum, também contém aminoácidos que mantêm a pele macia.Problemas de pele, como rugosidade e embotamento, devem -se em grande parte à falta de aminoácidos. Um estudo mostrou que a mistura de um aminoácido com uma pomada aliviada por queimaduras na pele, e as áreas afetadas retornaram ao seu estado normal sem se tornarem cicatrizes quenóides.
Verificou -se também que os aminoácidos são muito úteis para cuidar de cutículas danificadas.Cabelos secos e à moda podem indicar uma diminuição na concentração de aminoácidos em um estrato corneum gravemente danificado. Os aminoácidos têm a capacidade de penetrar na cutícula no eixo do cabelo e absorver a umidade da pele.Essa capacidade dos surfactantes à base de aminoácidos os torna muito úteis em xampus, corantes para o cabelo, amaciadores de cabelo, condicionadores de cabelo e a presença de aminoácidos torna o cabelo forte.
11 aplicações em cosméticos cotidianos
Atualmente, existe uma demanda crescente por formulações de detergentes à base de aminoácidos em todo o mundo.Sabe -se que os AAs têm melhor capacidade de limpeza, capacidade de espuma e propriedades de amolecimento de tecidos, o que os torna adequados para detergentes domésticos, xampus, lavagens corporais e outras aplicações.É relatado que um AAS anfotérico derivado do ácido aspártico é um detergente altamente eficaz com propriedades quelantes. Verificou-se que o uso de ingredientes detergentes que consistem em ácidos N-alquil-β-aminoetoxi reduzia a irritação da pele. Foi relatado que uma formulação de detergente líquido que consiste em N-cocoil-β-aminopropionato é um detergente eficaz para manchas de óleo nas superfícies metálicas. An aminocarboxylic acid surfactant, C 14 CHOHCH 2 NHCH 2 COONa, has also been shown to have better detergency and is used for cleaning textiles, carpets, hair, glass, etc. The 2-hydroxy-3-aminopropionic acid-N,N-acetoacetic acid derivative is known to have good complexing ability and thus gives stability to bleaching agents.
A preparação de formulações de detergente baseada em N- (acil-alanil-alanil-alanil-alanil-alanil-alanina de cadeia N'-Long foi relatada por Keigo e Tatsuya em sua patente por melhor capacidade de lavagem e estabilidade, quebra de espuma fácil e bom amolecimento do tecido. A Kao desenvolveu uma formulação de detergente baseada na n-acil-1-N-hidroxi-β-alanina e relatou baixa irritação na pele, alta resistência à água e alta potência de remoção de manchas.
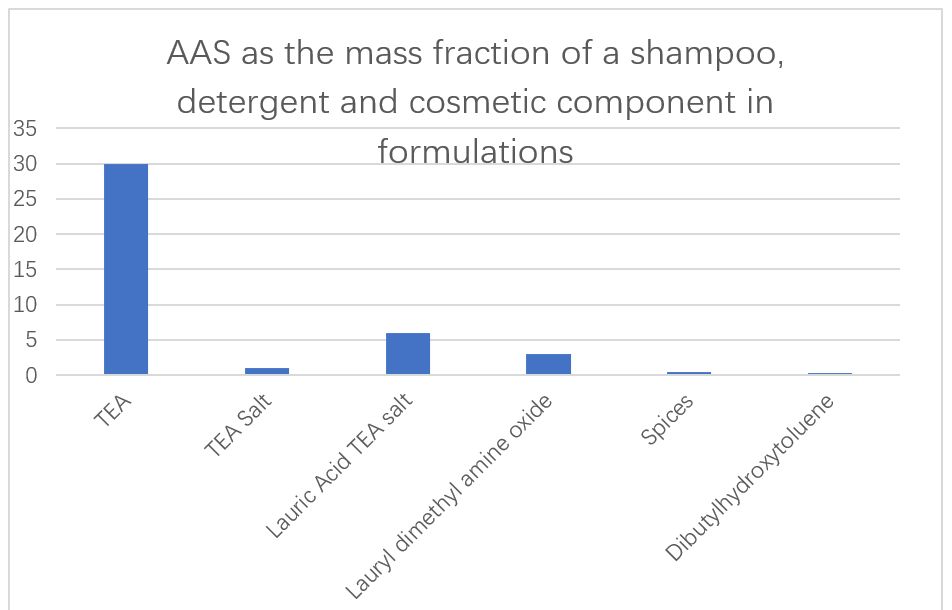
A empresa japonesa Ajinomoto usa AAs de baixo e facilmente degradável baseado em ácido L-glutâmico, L-arginina e L-lisina como os principais ingredientes em xampus, detergentes e cosméticos (Figura 13). A capacidade dos aditivos enzimáticos em formulações de detergentes para remover a incrustação de proteínas também foi relatada. AAs N-acil derivados de ácido glutâmico, alanina, metilglicina, serina e ácido aspártico foram relatados para seu uso como excelentes detergentes líquidos em soluções aquosas. Esses surfactantes não aumentam a viscosidade, mesmo em temperaturas muito baixas, e podem ser facilmente transferidas do navio de armazenamento do dispositivo de espuma para obter espumas homogêneas.
Hora de postagem: Jun-09-2022

